Vill du ha ett snabbt svar - sök i databasen
Nyckelord: specifik värmekapacitet
9 träffar
Fråga:
Hur kan det komma sig att det tar 20 minuter att koka en potatis i 100-gradigt vatten,
men att det tar drygt en timme att baka en potatis i en 250-gradig ugn?
Vänligen
Linda Eriksson
/Linda E, K-World, Stockholm 2000-03-10
Hur kan det komma sig att det tar 20 minuter att koka en potatis i 100-gradigt vatten,
men att det tar drygt en timme att baka en potatis i en 250-gradig ugn?
Vänligen
Linda Eriksson
/Linda E, K-World, Stockholm 2000-03-10
Svar:
Att koka potatis är i princip ett värmeöverföringsproblem. Det gäller att så snabbt som möjligt få en hög temperatur - uppåt 100oC i hela potatisen. Då sker en strukturomvandling (fråga [13169]) som gör potatisen mjuk.
Vatten är mycket effektivare för värmeöverföring än luft. Det beror på vattnets högre värmekapacitet, högre värmeledning och att strömningen blir intensiv vid kokning. Luft har mycket lägre värmekapacitet och värmeöverföringen luft-potatis är ineffektiv.
Se även fråga [16152].
Tänk på: Man kan sitta en god stund i en torrbastu vid 100 grader, men man tål absolut inte kokande vatten.
/KS/lpe 2000-03-11
Att koka potatis är i princip ett värmeöverföringsproblem. Det gäller att så snabbt som möjligt få en hög temperatur - uppåt 100oC i hela potatisen. Då sker en strukturomvandling (fråga [13169]) som gör potatisen mjuk.
Vatten är mycket effektivare för värmeöverföring än luft. Det beror på vattnets högre värmekapacitet, högre värmeledning och att strömningen blir intensiv vid kokning. Luft har mycket lägre värmekapacitet och värmeöverföringen luft-potatis är ineffektiv.
Se även fråga [16152].
Tänk på: Man kan sitta en god stund i en torrbastu vid 100 grader, men man tål absolut inte kokande vatten.
/KS/lpe 2000-03-11
Fråga:
1.Varför har vatten så hög specifik värmekapacitet?
2. Varför går det åt mer energi för att värma upp vatten än is?
Finns det något samband mellan smältpunkt och c?
/John T, Rudbeckianska, Västerås 2001-10-15
1.Varför har vatten så hög specifik värmekapacitet?
2. Varför går det åt mer energi för att värma upp vatten än is?
Finns det något samband mellan smältpunkt och c?
/John T, Rudbeckianska, Västerås 2001-10-15
Svar:
Många av vattnets märkliga egenskaper beror på vattenmolekylens stora
elektriska dipolmoment. Till exempel den höga värmekapaciteten.
Det är normalt att ett ämne har olika värmekapacitet i fast och i
smält form. Kolla svaren nedan! Slå gärna på vatten i
Nationalencyklopedin . Där finns en bra artikel.
. Där finns en bra artikel.
/KS 2001-10-15
Många av vattnets märkliga egenskaper beror på vattenmolekylens stora
elektriska dipolmoment. Till exempel den höga värmekapaciteten.
Det är normalt att ett ämne har olika värmekapacitet i fast och i
smält form. Kolla svaren nedan! Slå gärna på vatten i
Nationalencyklopedin
/KS 2001-10-15
Vad är specifik värmekapacitet?
Fråga:
Hej allihopa! Jag undrar om någon skulle kunna förklara vad specifik värmekapacitet är. När man på kurvan ser då man med konstant värme värmer på is som blir till vatten o sedan vattenånga ser man att själva funktionen är konstant, (först höjs temperaturern sedan går all värme åt att byta aggregations tillsånd osv), jag undrar om det finns ämnen där kurvan inte är konstant, utan exponentiell eller varierande helt enkelt.
/teresa k, norra real, stockholm 2008-05-13
Hej allihopa! Jag undrar om någon skulle kunna förklara vad specifik värmekapacitet är. När man på kurvan ser då man med konstant värme värmer på is som blir till vatten o sedan vattenånga ser man att själva funktionen är konstant, (först höjs temperaturern sedan går all värme åt att byta aggregations tillsånd osv), jag undrar om det finns ämnen där kurvan inte är konstant, utan exponentiell eller varierande helt enkelt.
/teresa k, norra real, stockholm 2008-05-13
Svar:
Hej Teresa!Specifik värmekapacitet är den mängd värme man måste tillföra för att höja temperaturen hos ett kg med en grad (1K). Om ämnet byter aggregationstillstånd (går från fast till flytande eller från flytande till gas), så går all energi år för att ändra aggregationstillståndet, och temperaturen är konstant. Specifik värmekapacitet för olika ämnen finns i Wikipedia, se länkar i fråga [14203].
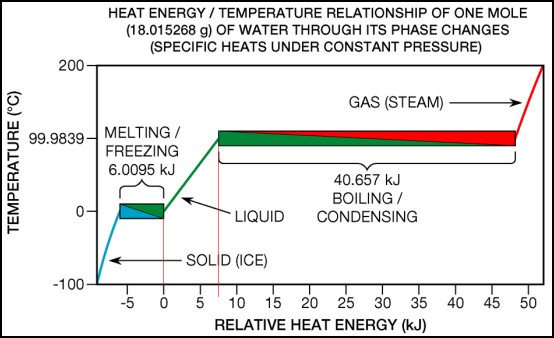
Se på figuren för vatten nedan (från Wikipedia-artikelnThermodynamic_temperature ). På den horisontella axeln är relativ tillförd värme och på den vertikala är temperaturen. Det finns två områden där kurvan är horisontell, dvs temperaturen konstant: när isen smälter och när vattnet kokar. Vidden på de konstanta områdena är ett mått på smältvärmet respektive ångbildningsvärmet. Den högra konstanta delen är 40.7 kJ/mol. Eftersom detta avser en mol, behöver vi räkna om värdet till kg (vattnet har molekylvikten 18 g/mol):
40.7 kJ/mol = 100040.7/18 = 2260 kJ/kg.
På samma sätt blir smältvärmet för is
6.01 kJ/mol = 10006.01/18 = 334 kJ/kg.
Från lutningen (egentligen 1/lutningen) hos den räta linjen mellan is och ånga kan man räkna ut den specifika värmekapaciteten för vatten:
7.5 kJ/(molK) = 10007.5/(18100) = 4.2 kJ/(kgK)
Det faktum att kurvan i detta område är en rät linje reflekterar det faktum att specifika värmekapaciteten för vatten är oberoende av temperaturen. Detta gäller approximativt för de flesta ämnen.
Sedan är jag inte helt klar över vad du menar att kurvan inte är konstant. I de horisontella områdena (vid smältpunkten 0oC och vid kokpunkten 100oC) ändras inte temperaturen om bara tillförseln av värmet sker på ett effektivt sätt. Då har hela provet en konstant temperatur och all tillförd värme går till att ändra aggregationstillstånd.
Den gröna kurvan mellan is och ånga representerar alltså den specifika värmekapaciteten för vatten. Det faktum att kurvan är mycket nära en rät linje betyder helt enkelt att vattens specifika värmekapacitet är konstant mellan 0oC och 100oC. Detta gäller inte allmänt - andra ämnen kan ha olika olinjära kurvor.
Man ser även på den blå kurvan till vänster (för is) att den avviker från en rät linje. Lägg också märke till att den blå kurvan har ungefär dubbelt så stor lutning som den gröna (för vatten). Detta betyder att specifika värmekapaciteten för is är ungefär hälften av den för vatten.
Hej Teresa!
Se på figuren för vatten nedan (från Wikipedia-artikeln
40.7 kJ/mol = 100040.7/18 = 2260 kJ/kg.
På samma sätt blir smältvärmet för is
6.01 kJ/mol = 10006.01/18 = 334 kJ/kg.
Från lutningen (egentligen 1/lutningen) hos den räta linjen mellan is och ånga kan man räkna ut den specifika värmekapaciteten för vatten:
7.5 kJ/(molK) = 10007.5/(18100) = 4.2 kJ/(kgK)
Det faktum att kurvan i detta område är en rät linje reflekterar det faktum att specifika värmekapaciteten för vatten är oberoende av temperaturen. Detta gäller approximativt för de flesta ämnen.
Sedan är jag inte helt klar över vad du menar att kurvan inte är konstant. I de horisontella områdena (vid smältpunkten 0oC och vid kokpunkten 100oC) ändras inte temperaturen om bara tillförseln av värmet sker på ett effektivt sätt. Då har hela provet en konstant temperatur och all tillförd värme går till att ändra aggregationstillstånd.
Den gröna kurvan mellan is och ånga representerar alltså den specifika värmekapaciteten för vatten. Det faktum att kurvan är mycket nära en rät linje betyder helt enkelt att vattens specifika värmekapacitet är konstant mellan 0oC och 100oC. Detta gäller inte allmänt - andra ämnen kan ha olika olinjära kurvor.
Man ser även på den blå kurvan till vänster (för is) att den avviker från en rät linje. Lägg också märke till att den blå kurvan har ungefär dubbelt så stor lutning som den gröna (för vatten). Detta betyder att specifika värmekapaciteten för is är ungefär hälften av den för vatten.
Varför bränner man sig på fyllningen i en pizza men inte på brödet?
Fråga:
Hej! Håller på med värme i skolan. I läroboken stod ett exempel om att man bränner sig i gommen på pizza därför att fyllningen kan lagra mer inre energi än brödet, men de har samma temperatur. Min lärare har sagt att saker känns olika varma och att man bränner sig på grund av att värmeöverföringen är olika för olika ämnen. Jag undrar ifall att man bränner sig beror på värmeöverföringen/konduktiviteten hos ämnet eller om det beror på specifika värmekapaciteten? Hänger detta ihop?
/Maria H, 2009-09-16
Hej! Håller på med värme i skolan. I läroboken stod ett exempel om att man bränner sig i gommen på pizza därför att fyllningen kan lagra mer inre energi än brödet, men de har samma temperatur. Min lärare har sagt att saker känns olika varma och att man bränner sig på grund av att värmeöverföringen är olika för olika ämnen. Jag undrar ifall att man bränner sig beror på värmeöverföringen/konduktiviteten hos ämnet eller om det beror på specifika värmekapaciteten? Hänger detta ihop?
/Maria H, 2009-09-16
Svar:
Hej Maria! Låt oss resonera systematiskt! Vad menas med att du bränner dig på gommen? Jo det är att gommen blir så varm (hög temperatur) att de värmekänsliga cellerna signalerar hög temperatur eller i värsta fall att man får en liten (övergående) skada. Det väsentliga är alltså att höja gommens temperatur.
För att höja gommens temperatur krävs dels att pizzan har tillräcklig specifik värmekapacitivitet och dels att värmeledningsförmågan är tillräcklig (och naturligtvis att den är tillräckligt varm). Så svaret är alltså: både och! Om värmeledningsförmågan är dålig, är det bara ett tunnt skikt som bidrar: liten temperaturhöjning eftersom temperatursänkningen hos pizzan är stor. Om specifika värmekapacitiviteten är liten, får man igen en stor sänkning av pizzans temperatur.
Metaller har mycket hög värmeledningsförmåga (eftersom det finns fria elektroner) och rimligt hög specifik värmekapacitivitet (värmemängd per kg och K). Man bränner sig alltså mycket på metaller. Du bränner dig på spiken i bastun men inte på trätrallorna. Du bränner dig inte heller på en het aluminiumfolie, eftersom massan är så liten och därmed värmekapaciteten.
Vatten har mycket hög specifik värmekapacitivitet och hygglig värmeledningsförmåga. Torra bitar som brödet har emellertid låg värmekapacitivitet och dålig värmeledningsförmåga eftersom brödet innehåller en massa luftbubblor som leder värme dåligt. Det är alltså på fyllningen (som innehåller mycket vatten) och inte på brödet du bränner dig.
/fa
Hej Maria! Låt oss resonera systematiskt! Vad menas med att du bränner dig på gommen? Jo det är att gommen blir så varm (hög temperatur) att de värmekänsliga cellerna signalerar hög temperatur eller i värsta fall att man får en liten (övergående) skada. Det väsentliga är alltså att höja gommens temperatur.
För att höja gommens temperatur krävs dels att pizzan har tillräcklig specifik värmekapacitivitet och dels att värmeledningsförmågan är tillräcklig (och naturligtvis att den är tillräckligt varm). Så svaret är alltså: både och! Om värmeledningsförmågan är dålig, är det bara ett tunnt skikt som bidrar: liten temperaturhöjning eftersom temperatursänkningen hos pizzan är stor. Om specifika värmekapacitiviteten är liten, får man igen en stor sänkning av pizzans temperatur.
Metaller har mycket hög värmeledningsförmåga (eftersom det finns fria elektroner) och rimligt hög specifik värmekapacitivitet (värmemängd per kg och K). Man bränner sig alltså mycket på metaller. Du bränner dig på spiken i bastun men inte på trätrallorna. Du bränner dig inte heller på en het aluminiumfolie, eftersom massan är så liten och därmed värmekapaciteten.
Vatten har mycket hög specifik värmekapacitivitet och hygglig värmeledningsförmåga. Torra bitar som brödet har emellertid låg värmekapacitivitet och dålig värmeledningsförmåga eftersom brödet innehåller en massa luftbubblor som leder värme dåligt. Det är alltså på fyllningen (som innehåller mycket vatten) och inte på brödet du bränner dig.
/fa

Test av mikrovågsugn
Fråga:
Jag har fått höra att man i framförallt USA testar mikrovågsugnar regelbundet (någon gång per år) för att se om de börjat läcka mikrovågor. Detta görs hemma genom att man kan hålla ett lysrör i närheten av mikron, lyser det så är ugnen för gammal och ska kasseras. Ligger någon som helst sanning i detta, att mikron kan bli gammal och börja läcka?
/Annika L, Lund 2010-02-05
Jag har fått höra att man i framförallt USA testar mikrovågsugnar regelbundet (någon gång per år) för att se om de börjat läcka mikrovågor. Detta görs hemma genom att man kan hålla ett lysrör i närheten av mikron, lyser det så är ugnen för gammal och ska kasseras. Ligger någon som helst sanning i detta, att mikron kan bli gammal och börja läcka?
/Annika L, Lund 2010-02-05
Svar:
Annika! Jag tror du blivit utsatt för ett skämt! Om det finns så mycket mikrovågor utanför ugnen att ett lysrör tänds, så är det mycket illa!
Mikovågorna hålls innne i ugnen genom att den är konstruerad som en faradaybur (se fråga [8879])
- solid metallplåt inne i ugnen och ett finmaskigt metallnät på luckan. Maskorna är betydligt mindre än mikrovågornas våglängd, så dessa kan inte slippa ut. Enda möjligheten är att dörren eller nätet skadats, men det kan man lätt se. Man behöver alltså inte testa om ungen läcker mikrovågor. Om man vill mäta strålningen (t.ex. för att testa en ny konstruktion) bör man ha mycket bättre mätapparatur än ett lysrör.
Se fråga [16041] om vad som händer med mikrovågsugnar när de blir gamla. Se mer om mikrovågsugnar:mikrovågsugn , länk 1 från strålsäkerhetsmyndigheten och länk 2.
Se fråga [3969] om hur effektiv faradayburen i en mikrovågsugn är.
Hur man kontrollerar effekten hos en mikrovågsugn
När mikrovågsugnen blir gammal blir magnetronen som genererar mikrovågorna mindre effektiv, och det tar längre tid att värma maten. Så här kan du kontrollera hur effektiv din mikrovågsugn är. Du behöver bara en skål (glas eller keramik) med 1 liter kallt vatten och en hyggligt exakt termometer.
Mät temperaturen på vattnet. Säg att vattnet är 20oC. Kör ugnen 1 minut. Mät vattentemperaturen igen. Säg att vattnet nu är 30oC. Sedan får vi räkna lite för att få fram effekten. Energin som krävs för att värma vattnet DT K är:
W = mcDT
där m är massan och c är vattnets specifika värmekapacitet 4180 J/(kg K).
Om vi kör mikron under tiden t får vi effekten
P = W/t = mcDT/t
1 liter vatten väger 1 kg, så effekten blir
P = 4180DT/t
Om vi körde mikron 1 minut och temperaturskillnaden var 10 K (eftersom vi har att göra med temperaturskillnader kan vi använda Celsius eller Kelvin) blir effekten
P = 418010/60 = 697 W
Om temperaturdifferensen blir liten bör man öka tiden t för att få bättre noggrannhet.
Den uppmätta effekten jämförs sedan med den nominella effekten enligt bruksanvisningen. Man kan även mäta in-effekten direkt med en wattmeter (seWatt_meter , bilden nedan). Om effekten är betydligt lägre än vad den skall vara är mikrovågsugnen skadad.
Om ovanstående är för krångligt kan man om man har en "standardportion", t.ex. ett fruset halvt franskbröd, helt enkelt se om upptiningen tar längre tid än vanligt.
Annika! Jag tror du blivit utsatt för ett skämt! Om det finns så mycket mikrovågor utanför ugnen att ett lysrör tänds, så är det mycket illa!
Mikovågorna hålls innne i ugnen genom att den är konstruerad som en faradaybur (se fråga [8879])
- solid metallplåt inne i ugnen och ett finmaskigt metallnät på luckan. Maskorna är betydligt mindre än mikrovågornas våglängd, så dessa kan inte slippa ut. Enda möjligheten är att dörren eller nätet skadats, men det kan man lätt se. Man behöver alltså inte testa om ungen läcker mikrovågor. Om man vill mäta strålningen (t.ex. för att testa en ny konstruktion) bör man ha mycket bättre mätapparatur än ett lysrör.
Se fråga [16041] om vad som händer med mikrovågsugnar när de blir gamla. Se mer om mikrovågsugnar:
Se fråga [3969] om hur effektiv faradayburen i en mikrovågsugn är.
Hur man kontrollerar effekten hos en mikrovågsugn
När mikrovågsugnen blir gammal blir magnetronen som genererar mikrovågorna mindre effektiv, och det tar längre tid att värma maten. Så här kan du kontrollera hur effektiv din mikrovågsugn är. Du behöver bara en skål (glas eller keramik) med 1 liter kallt vatten och en hyggligt exakt termometer.
Mät temperaturen på vattnet. Säg att vattnet är 20oC. Kör ugnen 1 minut. Mät vattentemperaturen igen. Säg att vattnet nu är 30oC. Sedan får vi räkna lite för att få fram effekten. Energin som krävs för att värma vattnet DT K är:
W = mcDT
där m är massan och c är vattnets specifika värmekapacitet 4180 J/(kg K).
Om vi kör mikron under tiden t får vi effekten
P = W/t = mcDT/t
1 liter vatten väger 1 kg, så effekten blir
P = 4180DT/t
Om vi körde mikron 1 minut och temperaturskillnaden var 10 K (eftersom vi har att göra med temperaturskillnader kan vi använda Celsius eller Kelvin) blir effekten
P = 418010/60 = 697 W
Om temperaturdifferensen blir liten bör man öka tiden t för att få bättre noggrannhet.
Den uppmätta effekten jämförs sedan med den nominella effekten enligt bruksanvisningen. Man kan även mäta in-effekten direkt med en wattmeter (se
Om ovanstående är för krångligt kan man om man har en "standardportion", t.ex. ett fruset halvt franskbröd, helt enkelt se om upptiningen tar längre tid än vanligt.

Vart tar de stora energimängderna vägen i ett vattenfall som INTE är reglerat?
Fråga:
Vart tar de stora energimängderna vägen i ett vattenfall som INTE är reglerat, dvs inte har något vattenfall? Blir det värme av alltihop, och i så fall borde det väl vara väldigt varmt vid vattenfallen och massor av vattenånga. Men är det så?
/Curt J, 2011-02-19
Vart tar de stora energimängderna vägen i ett vattenfall som INTE är reglerat, dvs inte har något vattenfall? Blir det värme av alltihop, och i så fall borde det väl vara väldigt varmt vid vattenfallen och massor av vattenånga. Men är det så?
/Curt J, 2011-02-19
Svar:
Ja, den potentiella energin blir värme. Låt oss räkna ut vad temperaturhöjningen blir. Vi har m kg vatten som faller 100 m. Potentiella energin (som blir rörelseenergi och sedan värme) är mgh.
Specifika värmekapaciteten C för vatten är 4180 J/kg.K, se fråga [14203]. Om vi kallar temperaturhöjningen DT får vi
mgh = mCDT
dvs
DT = gh/C = 10100/4180 = 0.24 K.
Dimensionskontroll: [(m/s2)m/(Nm)/(kgK)] =
[(m2/s2)/(kgm/s2m)/(kgK)] = [1/1/(K)] = [K]
Detta torde vara knappt mätbart!
/Peter E 2011-02-21
Ja, den potentiella energin blir värme. Låt oss räkna ut vad temperaturhöjningen blir. Vi har m kg vatten som faller 100 m. Potentiella energin (som blir rörelseenergi och sedan värme) är mgh.
Specifika värmekapaciteten C för vatten är 4180 J/kg.K, se fråga [14203]. Om vi kallar temperaturhöjningen DT får vi
mgh = mCDT
dvs
DT = gh/C = 10100/4180 = 0.24 K.
Dimensionskontroll: [(m/s2)m/(Nm)/(kgK)] =
[(m2/s2)/(kgm/s2m)/(kgK)] = [1/1/(K)] = [K]
Detta torde vara knappt mätbart!
/Peter E 2011-02-21
Specifik värmekapacitet
Fråga:
Försöker förstå sambandet mellan ett ämnes specifika värmekapacitet och dess densitet. Järn och trä har ungefär samma värmekapacitivtet men järn har mycket högre densitet och ledningsförmåga. Hur hänger det ihop? Jag funderar ochså över porslin jämfört med trä. Porslin har densitet 2,3kg/dm3 och värmekapacitivitet 0,8 kJ/kg.K. Har försökt hitta förklaringsmodeller om det hör ihop med bindningar mellan atomer/molekyler (förmåga att röra sig)? närhet mellan atomer/molekyler (förmåga att leda vidare) Men olika ämnens egenskaper säger mot varandra. Tacksam för förklaring som går att använda på högstadiet.
/Eva R, Sturebyskolan, Stockholm 2013-03-17
Försöker förstå sambandet mellan ett ämnes specifika värmekapacitet och dess densitet. Järn och trä har ungefär samma värmekapacitivtet men järn har mycket högre densitet och ledningsförmåga. Hur hänger det ihop? Jag funderar ochså över porslin jämfört med trä. Porslin har densitet 2,3kg/dm3 och värmekapacitivitet 0,8 kJ/kg.K. Har försökt hitta förklaringsmodeller om det hör ihop med bindningar mellan atomer/molekyler (förmåga att röra sig)? närhet mellan atomer/molekyler (förmåga att leda vidare) Men olika ämnens egenskaper säger mot varandra. Tacksam för förklaring som går att använda på högstadiet.
/Eva R, Sturebyskolan, Stockholm 2013-03-17
Svar:
Eva! Specifik värmekapacitet är ett ganska svårt ämne, så det finns inget enkelt svar på din fråga. Värme är ju slumpmässig rörelse hos molekyler, så den specifika värmekapaciteten bestäms inte av densiteten direkt utan i princip av antalet molekyler och antal frihetsgrader per molekyl. För det första så finns det inget samband mellan värmeledningsförmåga och specifik värmekapacitet. För värmeledningsförmåga se fråga [3874].
Först några definitioner:
Gaskonstanten (i allmänna gaslagen): R = 8.3145 J/(molK)
Boltzmanns konstant : k = 1.3806510-23 J/K
är en naturkonstant som relaterar temperatur för en mängd partiklar (molekyler) till energi på partikelnivå. Konstanten betecknas med kB eller bara k och motsvarar den allmänna gaskonstanten R dividerad med Avogadros tal NA.
Avogadros tal : NA = 6.022141023 /mol
är en fysikalisk konstant som anger antalet atomer eller molekyler i en mol av en substans.
R = kNA (k hänför sig alltså till en molekyl och R hänför sig till en mol, dvs NA molekyler)
(R = 1.3806510-236.022141023 = 8.3145)
För fasta ämnen och vätskor är det inte helt lätt, men låt oss börja med en gas eftersom det är lättare att förstå.
Figuren nedan (frånHeat_capacity ) visar värmekapaciteten CV för en tvåatomig gas (t.ex. N2) dividerat med gaskonstanten R som funktion av den absoluta temperaturen. För det första kan vi konstatera att CV varierar med temperaturen. Detta gäller oftast även för vätskor/fasta ämnen.
Varje frihetsgrad har värmekapaciteten (1/2)R J/mol eller (1/2)k J/partikel. Låt oss betrakta en tvåatomig gas, se figuren nedan. Molekylen kan röra sig i tre riktningar x,y och z. Vi har alltså 3 frihetsgrader och värmekapaciteten vid låga temperaturer blir (3/2)R.
Vid lite högre temperaturer kommer nya frihetsgrader in för en tvåatomig gas (för en enatomig gas förblir värmekapaciteten (3/2)R). Först rotation. En tvåatomig molekyl kan rotera kring två axlar. Den tredje axeln är linjen mellan de två atomerna, och den kommer inte i fråga av kvantmekaniska skäl (symmetri). Vi har alltså ytterligare två frihetsgrader, och vid normala temperaturer är CV = (5/2)R. (Figuren är lite missvisande här eftersom detta är temperaturområdet en tvåatomig gas normalt befinner sig i.)
Vid ytterligare högre temperatur kommer även vibrationer in. Molekylen kan vibrera längs axeln som definieras av linjen mellan atomerna. Denna vibration har två frihetsgrader (potentiell energi och kinetisk energi), så CV = (7/2)R.
Vad händer då med fasta ämnen/vätskor? Alla atomer binds till sina närmaste grannar. Vi bör alltså ha tre vibrationstillstånd (x, y och z) med två frihetsgrader var (potentiell energi och kinetisk energi). CV bör alltså vara
32 (1/2)R = 3R
Detta kallasDulong-Petits lag . Denna stämmer ganska väl för de flesta ämnen. Det tillkommer emellertid ett par komplikationer. För vissa ämnen, speciellt lätta ämnen med starka bindningar som C och Be, är vissa av vibrationstillstånden blockerade vid rumstemperatur eftersom excitationsenergin är för hög. Värmekapaciteten blir då lägre än 3R. Dessutom är det antalet atomer som bestämmer CV. I tabellen Heat_capacityTable_of_specific_heat_capacities ges CV i sista kolumnen i enheten J/(molKatom). Om man har ett sammansatt ämne i fast form måste man alltså multiplicera värdet med antalet atomer i en molekyl. Ta luft som exempel. Luft består till största delen av tvåatomiga molekyler. Vi måste alltså multiplicera det givna värdet 1.25 med antalet atomer i en luftmolekyl (2) för att få det korrekta värdet (5/2)R.
Eftersom vibrationstillstånden inte kan exciteras vid låg energi brukar CV för fasta ämnen gå mot noll när temperaturen går mot noll.
Se även fråga [17968].
Eva! Specifik värmekapacitet är ett ganska svårt ämne, så det finns inget enkelt svar på din fråga. Värme är ju slumpmässig rörelse hos molekyler, så den specifika värmekapaciteten bestäms inte av densiteten direkt utan i princip av antalet molekyler och antal frihetsgrader per molekyl. För det första så finns det inget samband mellan värmeledningsförmåga och specifik värmekapacitet. För värmeledningsförmåga se fråga [3874].
Först några definitioner:
är en naturkonstant som relaterar temperatur för en mängd partiklar (molekyler) till energi på partikelnivå. Konstanten betecknas med kB eller bara k och motsvarar den allmänna gaskonstanten R dividerad med Avogadros tal NA.
är en fysikalisk konstant som anger antalet atomer eller molekyler i en mol av en substans.
R = kNA (k hänför sig alltså till en molekyl och R hänför sig till en mol, dvs NA molekyler)
(R = 1.3806510-236.022141023 = 8.3145)
För fasta ämnen och vätskor är det inte helt lätt, men låt oss börja med en gas eftersom det är lättare att förstå.
Figuren nedan (från
Varje frihetsgrad har värmekapaciteten (1/2)R J/mol eller (1/2)k J/partikel. Låt oss betrakta en tvåatomig gas, se figuren nedan. Molekylen kan röra sig i tre riktningar x,y och z. Vi har alltså 3 frihetsgrader och värmekapaciteten vid låga temperaturer blir (3/2)R.
Vid lite högre temperaturer kommer nya frihetsgrader in för en tvåatomig gas (för en enatomig gas förblir värmekapaciteten (3/2)R). Först rotation. En tvåatomig molekyl kan rotera kring två axlar. Den tredje axeln är linjen mellan de två atomerna, och den kommer inte i fråga av kvantmekaniska skäl (symmetri). Vi har alltså ytterligare två frihetsgrader, och vid normala temperaturer är CV = (5/2)R. (Figuren är lite missvisande här eftersom detta är temperaturområdet en tvåatomig gas normalt befinner sig i.)
Vid ytterligare högre temperatur kommer även vibrationer in. Molekylen kan vibrera längs axeln som definieras av linjen mellan atomerna. Denna vibration har två frihetsgrader (potentiell energi och kinetisk energi), så CV = (7/2)R.
Vad händer då med fasta ämnen/vätskor? Alla atomer binds till sina närmaste grannar. Vi bör alltså ha tre vibrationstillstånd (x, y och z) med två frihetsgrader var (potentiell energi och kinetisk energi). CV bör alltså vara
32 (1/2)R = 3R
Detta kallas
Eftersom vibrationstillstånden inte kan exciteras vid låg energi brukar CV för fasta ämnen gå mot noll när temperaturen går mot noll.
Se även fråga [17968].

Uppvärmning av en pool
Fråga:
Vi håller precis på att värma vår nyfyllda pool. Det verkar ta jättelång tid, typ 2 grader per dygn. Mamma säger att det kommer gå fortare när poolen blivit lite varmare men pappa säger att det kommer fortsätta öka med ca 2 grader per dygn. Vem har rätt?
/Wilhelm S, Ellagårdsskolan, Täby 2014-02-05
Vi håller precis på att värma vår nyfyllda pool. Det verkar ta jättelång tid, typ 2 grader per dygn. Mamma säger att det kommer gå fortare när poolen blivit lite varmare men pappa säger att det kommer fortsätta öka med ca 2 grader per dygn. Vem har rätt?
/Wilhelm S, Ellagårdsskolan, Täby 2014-02-05
Svar:
Wilhelm! För en gångs skull är det pappa som har rätt! Värmemängden som krävs för att värma vattnet en grad är konstant mellan 0 och 100oC, dvs när vatten är flytande (se fråga [15734]). Om något kommer uppvärmningen gå långsammare eftersom förlusterna ökar med ökande temperaturskillnad vatten-luft.
En bassäng med vatten har mycket stor värmekapacitet, så det krävs mycket energi för att värma upp den. Låt oss anta följande:
Bassängens volym: 6x4x1.5 = 36 m3
Specifik värmekapacitet för vatten: 4.2 kJ/(kgK)
Energi för att värma vattnet en grad:
42003610001 = 151200000 = 1.5108 J
Om vi vill värma vattnet 2 grader per dygn behöver vi effekten:
2151200000/(246060) = 3500 W = 3.5 kW
2014-02-05
Wilhelm! För en gångs skull är det pappa som har rätt! Värmemängden som krävs för att värma vattnet en grad är konstant mellan 0 och 100oC, dvs när vatten är flytande (se fråga [15734]). Om något kommer uppvärmningen gå långsammare eftersom förlusterna ökar med ökande temperaturskillnad vatten-luft.
En bassäng med vatten har mycket stor värmekapacitet, så det krävs mycket energi för att värma upp den. Låt oss anta följande:
Bassängens volym: 6x4x1.5 = 36 m3
Specifik värmekapacitet för vatten: 4.2 kJ/(kgK)
Energi för att värma vattnet en grad:
42003610001 = 151200000 = 1.5108 J
Om vi vill värma vattnet 2 grader per dygn behöver vi effekten:
2151200000/(246060) = 3500 W = 3.5 kW
2014-02-05
Vad gör vissa ämnen supraledande?
Fråga:
Hej, jag undrar vad som gör vissa ämnen supraledande? Måste det finnas en halvmetall med? Och varför blir ämnen bara supraledande vid låga temperaturer?
Tacksam för svar!
/Johanna L, 2014-06-10
Hej, jag undrar vad som gör vissa ämnen supraledande? Måste det finnas en halvmetall med? Och varför blir ämnen bara supraledande vid låga temperaturer?
Tacksam för svar!
/Johanna L, 2014-06-10
Svar:
Wikipedia (Supraledare ) definierar supraledning:
) definierar supraledning:
Supraledning finns vid tillräckligt låga temperaturer hos vissa metaller och även keramiska ämnen. Det finns ämnen som är supraledande vid så hög temperatur att man kan använda billigt och lättillgängligt flytande kväve som kylmedel (kokpunkt 77 K).
Supraledning är ganska komplext och det finns olika förklaringar och fenomenet är inte helt förstått, speciellt när det gäller högtemperatursupraledare. Den klassiska förklaringen är BCS-teorin (seBCS_theory ).
I en vanlig ledare (typiskt en metall) sker laddningstransporten med fria elektroner, se fråga [9549]. Elektronerna kolliderar med atomerna i gittret och i en del av dessa kollisioner förlorar elektronen energi som värmer upp ledaren. Denna uppvärmning av ledaren är oftast oönskad eftersom den innebär en energiförlust (ledningsresistans).
I vissa ledare vid låg temperatur slår sig elektronerna ihop två och två med motsatt spinn (+1/2.-1/2). Man får då vad man kallar ett Cooper-par med spinnet 0. Dessa Cooper-par leder strömmen i stället för fria elektroner. På grund av kvantmekaniken är den emellertid två avgörande skillnader:
1 Eftersom ett Cooper-par har heltaligt spinn (0) är de bosoner och behöver till skillnad från fermioner (halvtaligt spinn) inte lyda pauliprincipen, se fråga [18298]. Alla Cooper-par kan då befinna sig i det lägsta tillståndet, grundtillståndet. Detta kallas Bose-Einstein-kondensat, se fråga [1136].
2 Energin i grundtillståndet är för liten för att Cooper-paren skall kunna växelverka med gittret. Detta betyder att kollisioner blir "förbjudna" och Cooper-paren kan röra sig obehindrat, det vill säga att resistansen är noll.
I figuren nedan visas resistiviteten (grön kurva) som funktion av temperaturen. Man ser att resistiviteten är exakt noll för temperaturer mindre än Tc. Den blå kurvan visar specifik värmekapacitet. Man ser att även denna påverkas vid fasövergången T=Tc.
Se ävenSuperconductivity .
Wikipedia (Supraledare
 ) definierar supraledning:
) definierar supraledning:Supraledning är ett fenomen i fasta tillståndets fysik som uppträder under en viss kritisk temperatur (ofta betecknad Tc) i vissa material. Ett supraledande material karakteriseras av sin oändligt stora elektriska ledningsförmåga och av att det inte kan innehålla något magnetiskt fält i innandömet (Meissnereffekten). Fenomenet förklaras teoretiskt av att elektronerna vid tillräckligt låga temperaturer parar ihop sig till Cooper-par.
Supraledning finns vid tillräckligt låga temperaturer hos vissa metaller och även keramiska ämnen. Det finns ämnen som är supraledande vid så hög temperatur att man kan använda billigt och lättillgängligt flytande kväve som kylmedel (kokpunkt 77 K).
Supraledning är ganska komplext och det finns olika förklaringar och fenomenet är inte helt förstått, speciellt när det gäller högtemperatursupraledare. Den klassiska förklaringen är BCS-teorin (se
I en vanlig ledare (typiskt en metall) sker laddningstransporten med fria elektroner, se fråga [9549]. Elektronerna kolliderar med atomerna i gittret och i en del av dessa kollisioner förlorar elektronen energi som värmer upp ledaren. Denna uppvärmning av ledaren är oftast oönskad eftersom den innebär en energiförlust (ledningsresistans).
I vissa ledare vid låg temperatur slår sig elektronerna ihop två och två med motsatt spinn (+1/2.-1/2). Man får då vad man kallar ett Cooper-par med spinnet 0. Dessa Cooper-par leder strömmen i stället för fria elektroner. På grund av kvantmekaniken är den emellertid två avgörande skillnader:
1 Eftersom ett Cooper-par har heltaligt spinn (0) är de bosoner och behöver till skillnad från fermioner (halvtaligt spinn) inte lyda pauliprincipen, se fråga [18298]. Alla Cooper-par kan då befinna sig i det lägsta tillståndet, grundtillståndet. Detta kallas Bose-Einstein-kondensat, se fråga [1136].
2 Energin i grundtillståndet är för liten för att Cooper-paren skall kunna växelverka med gittret. Detta betyder att kollisioner blir "förbjudna" och Cooper-paren kan röra sig obehindrat, det vill säga att resistansen är noll.
I figuren nedan visas resistiviteten (grön kurva) som funktion av temperaturen. Man ser att resistiviteten är exakt noll för temperaturer mindre än Tc. Den blå kurvan visar specifik värmekapacitet. Man ser att även denna påverkas vid fasövergången T=Tc.
Se även

Länkar till externa sidor kan inte garanteras bibehålla informationen som fanns vid tillfället när frågan besvarades.
Denna sida från NRCF är licensierad under Creative Commons: Erkännande-Ickekommersiell-Inga bearbetningar