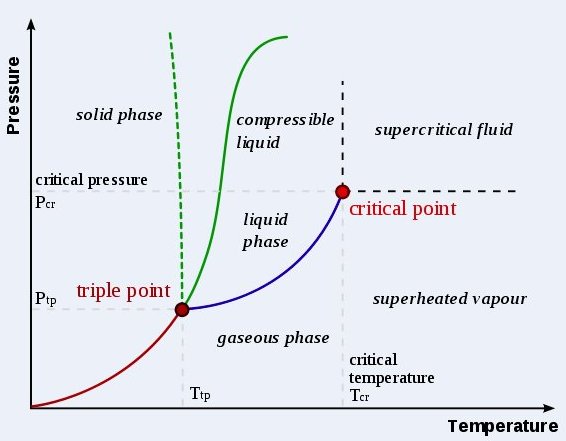
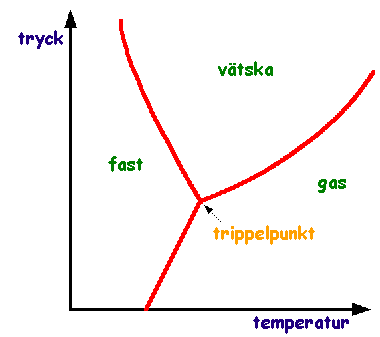
Vill du ha ett snabbt svar - sök i databasen: Anpassad Google-sökning 7 frĺgor/svar hittade Värme [19712] Svar: Vid högre temperaturer bildas istället plasma, och vid lĺga formar vissa ämnen Bose–Einstein-kondensat. Vid extremt högt tryck uppstĺr tillstĺndet degenererad materia. Aggregationstillstĺnd kallas ibland faser, men fas har en mer specifik betydelse. Diamant och grafit är tvĺ olika faser av grundämnet kol, men de är i samma aggregationstillstĺnd, nämligen fast, vid rumstemperatur. Fast form Partiklarna (joner, atomer eller molekyler) är packade tätt tillsammans. Krafterna mellan partiklarna är sĺ starka att partiklarna inte kan röra sig fritt, utan endast vibrera. Detta betyder att solid materia har en stabil, avgränsad form och en bestämd volym. Solid materia kan bara ändra form genom att man brukar vĺld mot den, till exempel bryter eller klipper den. Solid materia kan transformeras till flytande tillstĺnd (vätska) genom att man smälter den. Den kan ocksĺ förvandlas till gas genom sublimering. Flytande form Krafterna mellan molekylerna är viktiga, men molekylerna har tillräckligt med energi för att röra sig i relation till varandra och strukturen är rörlig. Det betyder att formen inte är bestämd, utan avgörs av den behĺllare vätskan befinner sig i. Hos en ideal vätska är volymen bestämd, sĺ länge temperaturen är konstant. I praktiken är dock vätskor i nĺgon mĺn kompressibla, dock lĺngt ifrĺn pĺ samma sätt som gaser. Gas Molekylerna har sĺ mycket rörelseenergi att krafterna mellan dem är smĺ (eller noll, hos en ideal gas) och molekylerna befinner sig lĺngt frĺn varandra. En gas har ingen bestämd form eller volym, men fyller upp hela den behĺllare de befinner sig i. En vätska kan transformeras till gas, om man vid konstant tryck värmer upp den till sin kokpunkt För att illustrera de olika aggegationstillstĺnden av ett ämne använder man sig av ett fasdiagram, se frĺga 17563 När det gäller vattnets egenskaper är de sĺ kallade vätebindningarna helt avgörande, se frĺga 17391 Generellt är bindningarna mellan atomer/molekyler i ett fast ämne mycket starka och de har fixerade vinklar i förhĺllande till varandra. Vid ökande temperatur vibrerar molekylerna mer och mer tills de förlorar vinkelberoendet och kan röra sig förbi varandra, vi har en vätska. Vi ännu högre temperatur blir vibrationerna sĺ vĺldsamma att molekylerna blir helt fria och vi har en gas, se nedanstĺende figur. Se även State_of_matter Nyckelord: vatten/is [49]; fasdiagram [7]; Värme [19681] Ursprunglig frĺga: Svar: 300 K (27oC) 3.6 kPa Vad som händer vid gränslinjen mellan gas och vätska är att vid ökande tryck och konstant temperatur kondenseras vattenĺngan till vatten. Därvid sjunker trycket tillbaka till det ursprungliga som motsvarar ĺngtrycket vid den givna temperaturen. Om man ökar trycket igen kondenseras mer ĺnga tills endast vatten ĺterstĺr. Se vidare Phase_diagram Nyckelord: fasdiagram [7]; kokande vatten [17]; Värme [19331] Kan man göra likadant med vatten som är varmare än 100 grader dĺ det ju blir ĺnga. Om man hĺller ĺngan under högt tryck blir den dĺ flytande vatten med en högre temperatur sĺ att man kan transportera den i en tank sĺ länge man hĺller trycket. Vilken temperatur mĺste vattnet ha för att man praktiskt skall kunna transportera det i en tank eller ett rör? Svar: Se vidare Critical_point_(thermodynamics) Nyckelord: fasdiagram [7]; Blandat [17563] Ursprunglig frĺga: Svar: Vi behöver även ett sĺ kallat fasdiagram som är en plot med temperatur pĺ x-axeln och tryck pĺ y-axeln där man markerar ämnets aggregationstillstĺnd (gas, vätska eller fast form) i diagrammet. I frĺga 12715 Lĺt oss som ett exempel utgĺ frĺn is med temperaturen -10oC och atmosfärstryck. Om vi ökar trycket lĺngsamt och hĺller temperaturen konstant, sĺ kommer isen att smälta vid trycket 113 Mpa (c:a 1100 atmosfärer) och sedan ĺtergĺ till is vid 443 MPa (c:a 4400 atmosfärer). Lĺt oss anta att vĺrt prov har en yta pĺ 1 cm2 = 0.0001 m2. Trycket 113 MPa [MN/m2] motsvarar dĺ kraften 0.0001*113*106 = 11300 N. Detta är en kraft pĺ 11300/g = ungefär 1000 kg. Vi behöver alltsĺ ĺstadkomma en kraft motsvarande ett ton för att smälta isen. Om isens temperatur är högre erfordras naturligvis mycket mindre kraft, för temperaturen -1oC fordras en kraft motsvarande 100 kg. Den klassiska förklaringen till varför is är halkigt är alltsĺ inte korrekt: trycket frĺn skridskoskenan är knappast tillräckligt för att smälta lite is och ge ett halkigt ytskikt av vattenmolekyler. Se länk 1 och 2 för alternativa förklaringar. Observera att isen har olika struktur i olika omrĺden. Stukturen i Ih är den normala som tar c:a 10% mer plats än vatten. I omrĺdet V har isen en annan struktur och betydligt högre densitet. Observera att axeln med densitet till höger avser flytande vatten. Nyckelord: fasdiagram [7]; vatten/is [49]; 1 http://www.nytimes.com/2006/02/21/science/21ice.html?_r=1 Materiens innersta-Atomer-Kärnor [16308] Vilken gas kan fĺ högst densitet vid sammanpressning, en lätt gas som helium (som borde kunna tryckas ihop mycket utan att kondensera) eller en tyngre gas som xenon (som har hög densitet frĺn början)? Svar: Det andra problemet är att det ovanför den kritiska temperaturen (se fasdiagrammet nedan frĺn Wikimedia Commons) inte är nĺgon skillnad pĺ gas och vätska, och under den kritiska temperaturen fĺr man en fasövergĺng gas till vätska när man ökar trycket vid konstant temperatur. I Wikipedia-artikeln om fasdiagram Phase_diagram Nyckelord: fasdiagram [7]; Blandat [12840] Svar: Bilden nedan visar ett förenklat "fasdiagram". Med ett sĺdant diagram (som baseras pĺ experimentella observationer) kan man ta reda pĺ i vilket aggregationstillstĺnd (fast form, vätska eller gasform) ett ämne kommer att befinna sig i vid ett visst tryck och temperatur. Man kan se att det under vissa betingelser sker en direkt övergĺng mellan gas och fast form, medan det i andra fall är gynnsammast (ur energisynpunkt) att gĺ via en vätskefas. I den s.k. trippelpunkten kan alla tre aggregationstillstĺnd existera samtidigt, se Triple_point Nyckelord: fasdiagram [7]; trippelpunkt [2]; Blandat [12715] a) Tänk nu att man har en behĺllare som rymmer ca en liter vatten. Behĺllaren har tjocka väggar–ca en meter- gjorda av ett mycket fast material. Om man nu sänker temperaturen under noll grader Celsius pĺ denna anordning, är det dĺ möjligt att fĺ vattnet att inte frysa till is tack vare att väggarna inte utvidgar sig. b) Om nu vattnet inte fryser till is fĺr dĺ vattnet samma temperatur som anordningen eller borde vattnet bli varmare? c) Här kommer en frĺga om ISBJÖRNAR ocksĺ:
1)Vad kan anledningen vara till att isbjörnens hud är svart? Kan det vara för att fĺ ut kroppens värme ända ut i huden?
Svar: För frĺga a och b fĺr vi hänvisa till fasdiagrammet frĺn
Water Structure and Science Den sista frĺgan är väl knappast en fysikfrĺga. Om det är sant att isbjörnarnas hud är svart skulle det kunna bero pĺ deras nära släktskap med brunbjörnen. Nyckelord: fasdiagram [7]; vatten/is [49]; Frĺgelĺdan innehĺller 7624 frĺgor med svar. ** Frĺgelĺdan är stängd för nya frĺgor tills vidare **
|



 Sök i svenska Wikipedia:
Sök i svenska Wikipedia:
