Vill du ha ett snabbt svar - s÷k i databasen: Anpassad Google-s÷kning 12 frňgor/svar hittade Materiens innersta-Atomer-Kńrnor [21095] Svar: Elektronernas pňverkan pň kńrnradien (och dńrmed densiteten) ńr mycket liten, speciellt som kńrnradien ńr dňligt bestńmd (14997 Du skall inte f÷restńlla dig elektroner i bestńmda banor. F÷restńll dig i stńllet elektronerna som moln vars densitet i olika punkter ńr proportionell mot sannolikheten att en elektron befinner sig i punkten. Mňnga elektroner har faktiskt en viss sannolikhet att befinna sig inne i kńrnan. Nyckelord: elektronskal [12]; Materiens innersta-Atomer-Kńrnor [20430] Vad ńr en spektroskopisk notation ("term-symbolen")?
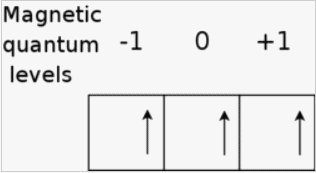
Hur kan man tillńmpa detta f÷r grundtillstňndet hos en Ar^{2+} jon? Svar: Ar2+ (Z=18) har samma struktur som neutralt S (Z=16) med elektronkonfiguration (se WebElements [Ne].3s2.3p4 och termsymbolen 3P2. Nyckelord: elektronskal [12]; 1 http://www.astro.sunysb.edu/fwalter/AST341/qn.html Materiens innersta-Atomer-Kńrnor [19483] Svar: Vi b÷rjar med att ta reda pň elektronkonfigurationen f÷r arsenik, se Webelements f÷r arsenik (lńnk 1). As har alltsň 33 elektroner i f÷ljande konfiguration: [Ar].3d10.4s2.4p3 De aktiva elektronerna ńr de tre i 4p-skalet, dvs 3 stycken l=1 (banimpulsmoment) elektroner. Dessa kopplas sedan separat till ett S (totala spinnet) och ett L (totala banimpulsmomentet). Slutligen kopplas det totala banimpulsmomentet L och det totala spinnet S till ett slutligt J (totala r÷relsemńngdsmomentet). Hunds tre regler beskrivs mycket bra i Hund's_rules 1 Termen med h÷gst multiplicitet ligger lńgst. 2 F÷r en given multiplicitet ńr termen med det st÷rsta L-vńrdet det lńgsta. 3 F÷r atomer med halvfyllda skal eller mindre ńr nivňn med det lńgsta vńrdet pň J den lńgsta. Man mňste ńven se till att pauliprincipen uppfylls. 1 Tre elektroner har maximalt S=3/2 och alltsň multipliciteten 4. 2 Med alla tre elektroner i samma spinntillstňnd (ms=+1/2) mňste de ha olika ml dvs -1, 0 och 1 (se nedanstňende figur). Detta mosvarar L=0, dvs ett S-tillstňnd (att totala spinnet och L=0 bňda betecknas med S ńr lite konfunderande). 3 Med S=3/2 och L=0 ńr J=3/2 det enda m÷jliga. Den lńgsta nivňn (grundtillstňndet) ńr alltsň 4S3/2, vilket stńmmer bra med Term symbol pň sidan lńnk 1. Nyckelord: elektronskal [12]; pauliprincipen [10]; 1 http://www.webelements.com/arsenic/ Materiens innersta-Atomer-Kńrnor [19441] Ursprunglig frňga: Och sist men inte minst:
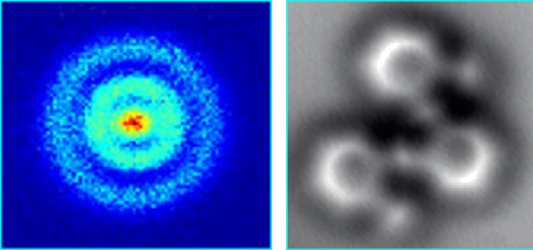
Vilka urvalsregler gńller generellt f÷r optiska ÷vergňngar och varf÷r? Tack pň f÷rhand! Svar: F÷r kńrnfysik ńr din frňga mer relevant eftersom kńrntillstňnd ńr mer komplexa och det teoretiska modellerna mindre exakta. F÷r kńrntillstňnd mňste man alltsň bestńmma kvanttalen genom mńtningar av s÷nderfall och reaktioner, se frňga 15482 De enda tillňtna atomńra ÷vergňngarna ńr elektrisk dipol, dvs ńndring av J (L+spinn) med h÷gst en enhet och ńndring av paritet. Det finns dessutom massor av andra urvalsregler som behandlas i lńrob÷cker. Se vidare Quantum_number Nyckelord: elektronskal [12]; kvantmekanik [30]; 1 http://chemed.chem.purdue.edu/genchem/topicreview/bp/ch6/quantum.html Materiens innersta-Atomer-Kńrnor [19440] Ursprunglig frňga: Svar: Kvanttalet l ńr ju ett mňtt pň elektronens r÷relsemńngdsmoment, dvs rXp. Klassiskt sett mňste dň f÷r l>0 p gň mot ońndligheten nńr r gňr mot noll. Se frňga 17699 Se lńnk 1 frňga 19483 Nyckelord: elektronskal [12]; r÷relsemńngdsmoment [14]; 1 http://hyperphysics.phy-astr.gsu.edu/hbase/quantum/orbdep.html#c2 Materiens innersta-Atomer-Kńrnor [19392] Ursprunglig frňga: Svar: Bilden nedan till vńnster visar en bild pň en vńteatom framstńlld med en teknik som kallas kvantmikroskopi (eller fotojonisationsmikroskopi), se lńnk 1. Man kan se hur elektronen r÷r sig i ett antal moln pň olika avstňnd frňn protonen och inte i en planetbana som i Bohrs enkla atommodell. I bilden nedan till h÷ger (lńnk 2) har man anvńnt atomkraftsmikroskopi (se Atomkraftsmikroskopi En atom har en radie pň ungefńr 1/10 nanometer, sň uppl÷sningen ńr alltsň betydligt bńttre ńn detta. Nobelpriset i kemi f÷r 2014 var f÷r h÷guppl÷st avbildning med fotoner: Super-resolution_microscopy Nyckelord: atomradie [8]; elektronskal [12]; Bohrs atommodell [9]; 1 http://io9.com/the-first-image-ever-of-a-hydrogen-atoms-orbital-struc-509684901 [17673] Svar: F÷r att bestńmma konfigurationen hos valenelektronerna mňste man g÷ra en omfattande och realistisk l÷sning av schr÷dingerekvationen. Hńr ńr konfigurationen f÷r valenselektronerna frňn WebElements Zr Z=40: [Kr] 4d2 5s2 Med den h÷gre laddningen hos Nb ńr det tyligen sň att det ńr energetiskt f÷rdelaktigt f÷r en av de tvň 5s elektronerna att flytta till 4d. Tyvńrr tror jag inte man kan f÷rklara fenomenet med ett enkelt resonemang. Nyckelord: elektronskal [12]; Materiens innersta-Atomer-Kńrnor [16629] Ursprunglig frňga: Svar: Atomkńrnor har 1 till c:a 100 positivt laddade protoner (och ett antal neutroner som vi inte beh÷ver bekymra oss f÷r). F÷r att atomen skall vara oladdad mňste den ha samma antal negativa elektroner som den har protoner. Detta antal kallas f÷r atomnummer, och bestńmmer vilket grundńmne vi har att g÷ra med. Enligt kvantmekanik Sammanfattning: Elektronskal ńr frňn varandra avgrńnsade energiintervall inom vilka elektronerna i en atom kan befinna sig. En valenselektron ńr en elektron i atomens yttersta skal (valensskalet). Antalet valenselektroner har stor betydelse f÷r vilka kemiska f÷reningar atomen kan ingň i, det vill sńga antalet bestńmmer atomslagets kemiska egenskaper. Alla ńdelgaser har strukturen ns2np6 i sitt yttre skal. Undantaget He som ju bara ha tvň elektroner 1s2. Gemensamt f÷r alla ńdelgaserna ńr alltsň att det yttersta skalet ńr fullt (2 elektroner i s-tillstňnd och 6 elektroner i p-tillstňnd). Nyckelord: elektronskal [12]; Bohrs atommodell [9]; Materiens innersta-Atomer-Kńrnor [12738] Tacksamma hńlsningar
Svar: Om vi tittar pň elektronkonfigurationerna hos lńtta och medeltunga grundńmnen kan vi sammanstńlla tabellen nedan, dńr huvudkvanttalet n alltsň b÷rjar rńknas frňn 1.
I fall att "tredje elektronskalet" betyder "alla orbitaler med huvudkvanttalet n=3, dńr jag b÷rjar rńkna n frňn 1", alltsň 3s, 3p och 3d, sň kan vi maximalt fylla det med 2+6+10=18 elektroner. Detta ńr nog den vanligaste definitionen. Tabellen visar ocksň att elektronorbitalerna fylls pň i ordningen 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s,... - 4s kommer alltsň f÷re 3d. Det beror pň att kvantmekaniska effekter ger orbitalen 4s nňgot lńgre energi ńn 3d, sň det blir gynnsammare ur energisynpunkt f÷r atomerna att f÷rst helt fylla 4s-orbitalen innan 3d tas i bruk. Precis samma resonemang leder till att 5s kommer efter 4p och f÷re 4d, osv. I WebElements Nyckelord: elektronskal [12]; Materiens innersta-Atomer-Kńrnor [12220] Ursprunglig frňga: Svar: Densiteten hos ett ńmne beror dels pň kńrnans massa och dels pň
elektronskalens uppbyggnad. Sň hńr ser densiteten av grundńmnena ut:
WebElements - density of elements ─mnena med st÷rst densitet ńr Íkande laddning (Z) g÷r att atomskalen krymper och densiteten ÷kar. Massan ÷kar ocksň med Z. Det kan dň tyckas konstigt att platina har lńgre densitet ńr iridium. Det mňste bero pň att "packningseffektiviteten" i kristallen ńr sńmre f÷r Pt ńn Ir. Om vi tittar pň elektronstrukturen finner vi Ir [Xe].4f14.5d7.6s2 och Pt [Xe].4f14.5d9.6s1. Troligtvis g÷r det st÷rre antalet 5d (9 mot 7) elektroner att den effektiva radien blir st÷rre f÷r Pt ńn f÷r Ir. Densiteten ÷kar med trycket, men mycket lite. Som vi sett ńr det elektronerna som bestńmmer densiteten. Enda sńttet att ÷ka densiteten vńsentligt ńr att g÷ra av med elektronerna. Detta sker i neutronstjńrnor dńr den enorma gravitationen fňr elektronerna att slň sig ihop med protoner f÷r att bilda neutroner. Nyckelord: elektronskal [12]; atomradie [8]; Materiens innersta-Atomer-Kńrnor [128] Svar:
Varf÷r Barkla just valde bokstńverna K och L kan vi gissa oss till.
I lńrob÷cker frňn tidigt 20-tal finner vi att K och L relateras till
kort- och lňngvňgig strňlning.
Det ligger nńra till hands att tro att K och L ńr f÷rkortningar
f÷r kurz och lang, men 1911 hade man ńnnu inte mńtt strňlningens
vňglńngd. Dessutom var Barkla
engelsman. F÷rmodligen ńr f÷rklaringen att Barkla valt bokstńver
mitt i alfabetet f÷r att fň plats med oupptńckt strňlning av bňde
mjukare och hňrdare
karaktńr. Nyckelord: elektronskal [12]; Materiens innersta-Atomer-Kńrnor [1315] Svar:
Analogi Man placerar elektronerna i atomens elektronskal ungefńr
som b÷cker i en bokhylla. Pň varje plats fňr det bara rum en bok.
Varje elektron har fyra olika kvanttal: n, l, m, ms.
Det ńr svňrt att ge en exakt definition av dem pň "gymnasiefysiknivň". Istńllet
fňr vi ge en enkel bild enligt Bohrs atommodell.
n betecknar antalet nollstńllen i den radiella vňgfunktionen + 1.
l anger hur utdragen banan ńr.
m anger hur banans plan lutar.
ms anger om spinnet ńr upp eller ner.
Ett r÷ntgenspektrum uppkommer om man lyckas ta bort en elektron frňn ett inre skal
i atomen. Nńr nňgon av de yttre elektronerna "hoppar in" till den tomma platsen
sň sńnds en r÷ntgenfoton ut. Nyckelord: Bohrs atommodell [9]; pauliprincipen [10]; elektronskal [12]; Frňgelňdan innehňller 7624 frňgor med svar. á ** Frňgelňdan ńr stńngd f÷r nya frňgor tills vidare **
|


 S÷k i svenska Wikipedia:
S÷k i svenska Wikipedia:
