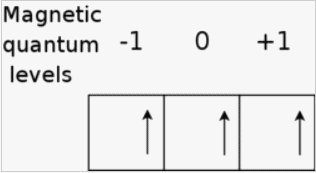
Materiens innersta-Atomer-Kärnor [19483] Svar: Vi börjar med att ta reda pĺ elektronkonfigurationen för arsenik, se Webelements för arsenik (länk 1). As har alltsĺ 33 elektroner i följande konfiguration: [Ar].3d10.4s2.4p3 De aktiva elektronerna är de tre i 4p-skalet, dvs 3 stycken l=1 (banimpulsmoment) elektroner. Dessa kopplas sedan separat till ett S (totala spinnet) och ett L (totala banimpulsmomentet). Slutligen kopplas det totala banimpulsmomentet L och det totala spinnet S till ett slutligt J (totala rörelsemängdsmomentet). Hunds tre regler beskrivs mycket bra i Hund's_rules 1 Termen med högst multiplicitet ligger lägst. 2 För en given multiplicitet är termen med det största L-värdet det lägsta. 3 För atomer med halvfyllda skal eller mindre är nivĺn med det lägsta värdet pĺ J den lägsta. Man mĺste även se till att pauliprincipen uppfylls. 1 Tre elektroner har maximalt S=3/2 och alltsĺ multipliciteten 4. 2 Med alla tre elektroner i samma spinntillstĺnd (ms=+1/2) mĺste de ha olika ml dvs -1, 0 och 1 (se nedanstĺende figur). Detta mosvarar L=0, dvs ett S-tillstĺnd (att totala spinnet och L=0 bĺda betecknas med S är lite konfunderande). 3 Med S=3/2 och L=0 är J=3/2 det enda möjliga. Den lägsta nivĺn (grundtillstĺndet) är alltsĺ 4S3/2, vilket stämmer bra med Term symbol pĺ sidan länk 1. Nyckelord: elektronskal [12]; pauliprincipen [10]; 1 http://www.webelements.com/arsenic/ Frĺgelĺdan innehĺller 7624 frĺgor med svar. ** Frĺgelĺdan är stängd för nya frĺgor tills vidare **
|