Vill du ha ett snabbt svar - sök i databasen
Nyckelord: Bohrs atommodell
4 träffar
Jag har några frågor angående Pauliprincipen, vad innebär den?
Vad betecknar elektronernas olika kvanttal för något? Vad är ett
röntgenspektrum och hur uppkommer det?
/Cecilia K, Katedral, Växjö 1998-04-01
Enligt kvantmekaniken kan en elektron i atomens elektronkal endast befinna sig i vissa tillstånd. Enligt
Pauliprincipen kan två elektroner aldrig befinna sig i samma tillstånd.
Analogi Man placerar elektronerna i atomens elektronskal ungefär
som böcker i en bokhylla. På varje plats får det bara rum en bok.
Varje elektron har fyra olika kvanttal: n, l, m, ms.
Det är svårt att ge en exakt definition av dem på "gymnasiefysiknivå". Istället
får vi ge en enkel bild enligt Bohrs atommodell.
n betecknar antalet nollställen i den radiella vågfunktionen + 1.
l anger hur utdragen banan är.
m anger hur banans plan lutar.
ms anger om spinnet är upp eller ner.
Ett röntgenspektrum uppkommer om man lyckas ta bort en elektron från ett inre skal
i atomen. När någon av de yttre elektronerna "hoppar in" till den tomma platsen
så sänds en röntgenfoton ut.
/GO 1998-04-09
Vad gjorde Ernest Rutherford mer ingående och vad fick han nobelpriset för?
/Per P, Artediskolan, Nordmaling 1998-05-05
Han var den som gjorde de experiment som visar hur atomen är uppbyggd. I detta
experiment sköt han alfapartiklar mot ett tunt folie och kom fram till att huvuddelen av atomens massa var koncentrerad i en kärna som är 1/10000 del av kärnans storlek. Bohr kompetterade sedan modellen med att det är elektroner som rör sig runt kärnan och bestämmer till en stor del atomens egenskaper.
Fundera: Antag att du är en skurk i vilda västern. Det kommer
en prärievagn som du tror är lastad med bomull. För att testa detta skjuter
du
hundra skott mot vagnen. 99 skott går rakt igenom vagnen medan ett studsar
tillbaks mot dig. Var vagnen lastad med bomull? Vad tror du vagnen var
lastad med?
Rutherfors experiment liknar mycket exemplet ovan. Han blev väldigt förvånad
när nästan, men inte riktigt, alla alfapartiklarna gick rakt igenom foliet. Han tolkade detta
som att
nästan allt är tomrum men att det finns små, men mycket tunga atomkärnor
mitt inne i atomen.
Det var han som formulerade atommodellen som säger att det finns en liten
men tung kärna i mitten.
Han fick Nobelpriset i kemi 1908 för tidigare arbeten om sönderfall av atomkärnor, se The Nobel Prize in Chemistry - Laureates![]() .
.
/GO/lpe 1998-11-16
Valenselektroner och elektronskal
Jag undrar hur man kan på bästa sätt förklara vad ett valenselektroner är och vad är ett elektronskal.
/Malin J, Ljungbacken, lidingö 2009-11-17
Malin! Är du inte lite ung för att fundera på elektronskal och valenselektroner? :-)
Atomkärnor har 1 till c:a 100 positivt laddade protoner (och ett antal neutroner som vi inte behöver bekymra oss för). För att atomen skall vara oladdad måste den ha samma antal negativa elektroner som den har protoner. Detta antal kallas för atomnummer, och bestämmer vilket grundämne vi har att göra med.
Enligt
Sammanfattning:
En
/Peter E 2009-11-17
Hur väl kan man avbilda en atom?
På samma sätt som en färgad pixel på datorn byter plats och det då ser ut som det rör sig på datorn, hur lite kan en atom röra sig? Alltså, vad är minsta avståndet som en atom rör sig för att faktiskt ha rört sig?
/Sixten F, Alléskolan, Floda 2014-05-02
Hej Sixten! Jag är inte helt säker på vad du menar. Jag antar du vill veta hur väl kan man avbilda en atom. Det finns numera flera olika metoder att avbilda atomer.
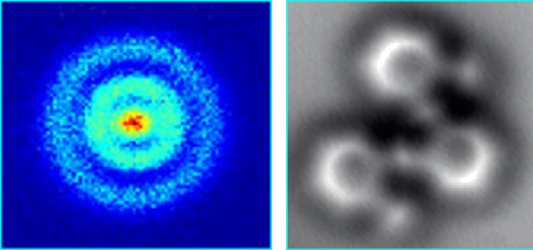
Bilden nedan till vänster visar en bild på en väteatom framställd med en teknik som kallas kvantmikroskopi (eller fotojonisationsmikroskopi), se länk 1. Man kan se hur elektronen rör sig i ett antal moln på olika avstånd från protonen och inte i en planetbana som i Bohrs enkla atommodell.
I bilden nedan till höger (länk 2) har man använt atomkraftsmikroskopi (se Atomkraftsmikroskopi
 ) för att avbilda en molekyl bestående av kolatomer och väteatomer. Man kan tydligt se att kolatomerna förekommer i sexkantiga bensenringar.
) för att avbilda en molekyl bestående av kolatomer och väteatomer. Man kan tydligt se att kolatomerna förekommer i sexkantiga bensenringar. En atom har en radie på ungefär 1/10 nanometer, så upplösningen är alltså betydligt bättre än detta.
Nobelpriset i kemi för 2014 var för högupplöst avbildning med fotoner:
Länkar till externa sidor kan inte garanteras bibehålla informationen som fanns vid tillfället när frågan besvarades.
Denna sida från NRCF är licensierad under Creative Commons: Erkännande-Ickekommersiell-Inga bearbetningar