Visa frĺga/svar
Materiens innersta-Atomer-Kärnor [16308]
Frĺga:
Densiteten för en "ideal" gas borde kunna bli högre än densiteten för en vätska, bara det är tillräckligt högt tryck. Om vi antar att gasen inte löser sig i vattnet, och inte kondenseras till vätska av det höga trycket, skulle vi dĺ kunna fĺ gasbubblor som stannar kvar pĺ havsbottnen?
Vilken gas kan fĺ högst densitet vid sammanpressning, en lätt gas som helium (som borde kunna tryckas ihop mycket utan att kondensera) eller en tyngre gas som xenon (som har hög densitet frĺn början)?
/Michael d, Rodengymnasiet, Norrtälje
Svar:
Det är tvĺ problem med ditt resonemang. För det första är en gas vid högt tryck ingen ideal gas - molekylerna är sĺ tätt ihop att de pĺverkar varandra.
Det andra problemet är att det ovanför den kritiska temperaturen (se fasdiagrammet nedan frĺn Wikimedia Commons) inte är nĺgon skillnad pĺ gas och vätska, och under den kritiska temperaturen fĺr man en fasövergĺng gas till vätska när man ökar trycket vid konstant temperatur.
I Wikipedia-artikeln om fasdiagram Phase_diagram 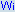 sägs att
sägs att
In the diagram, the phase boundary between liquid and gas does not continue indefinitely. Instead, it terminates at a point on the phase diagram called the critical point. This reflects the fact that, at extremely high temperatures and pressures, the liquid and gaseous phases become indistinguishable, in what is known as a supercritical fluid.
/Peter ENyckelord: fasdiagram [7];
*
Frĺgelĺdan innehĺller 7624 frĺgor med svar.
Senaste ändringen i databasen gjordes 2022-05-21 17:33:39.
** Frĺgelĺdan är stängd för nya frĺgor tills vidare **
sök | söktips | Veckans frĺga | alla 'Veckans frĺga' | ämnen | dokumentation | ställ en frĺga
till diskussionsfora