Vill du ha ett snabbt svar - sök i databasen: Anpassad Google-sökning 25 frĺgor/svar hittade Värme [21195] Svar: Se frĺga 21140 Nyckelord: specifik värmekapacitet [25]; Värme [21140] Specifik värmekapacitet för stĺl är 460J /(kg x K) Svar: (100-20)*1.8*4180 = 601900 J Om starttemperaturen hos stĺlkastrullen är T grader blir det tillgängliga energin (T-100)*0.8*460 = (T-100)*368 Om vi sätter dessa lika fĺr vi (T-100) = 601900/368 = 1636 alltsĺ T = 1736 grader Med tanke pĺ att smältpunkten hos stĺl är max 1500 grader (se länk 1) är det föreslagna kokmetoden inte särskilt realistisk. Kastrullen kommer att smälta och vattnet förĺngas. Nyckelord: specifik värmekapacitet [25]; Värme [21012] Varje gĺng man kokar pasta häller man ju ur massa kokande vatten. Den är ju uppvärmd och förutom att man kastar bort vatten är ju det ocksĺ värme energi. Samma eg med en torktumlares vatten behĺllare. Sĺ nu till frĺgan. Om man har 1 liter kokande vatten, kan man räkna ut hur mycket energi som ligger "lagrat" I detta? helst skulle man vilja ha det i Kwh/watt för att kanske kunna jämföra med tex ett element för värma upp rummet lika mycket.. gĺr det och/eller behöver man vara fysiker för att förstĺ ;) Svar: Värmeinnehĺllet blir dĺ 1*80*4.180 = 334 kJ = 334 kWs = 334/3600 = 0.093 kWh Det är inte mycket, sĺ det är knappast lönt att utvinna energin i pastavattnet. För t.ex. industroprocesser kan det emellertid vara lönsamt att ĺtervinna energi frĺn avloppet med en värmepump. Se vidare länk 1 och länk 2. Nyckelord: specifik värmekapacitet [25]; värmepump/kylskĺp [8]; 1 http://www.energi-miljo.se/energi-miljo/varmeatervinning-ur-avloppet Värme [20997] Svar: Se Specifik_värmekapacitet Det fins flera orsaker (se länk 1 och 2 nedan). 1 Den specifika värmekapaciteten definieras som mängden värme som krävs per kg för att höja temperaturen med en grad. Eftersom molekylvikten för vatten är ganska lĺg (18 enheter) kommer 1 kg vatten att innehĺlla mĺnga mol (och därmed molekyler) och fĺr därmed hög specifik värmekapacitet. 2 Det gĺr ĺt mycket energi för att bryta upp vätebindningarna som orsakas av den bipolära strukturen hos vattenmolekylen, se frĺga 20746 3 Vattenmolekylen har tre frihetsgrader för rotation och därtill flera vibrations-frihetsgrader. När vattnet värms upp lagras en del av energin i dessa rotations-vibrations tillstĺnd, vilket ger en hög värmekapacitet. Nyckelord: vatten/is [49]; specifik värmekapacitet [25]; 1 https://chemistry.stackexchange.com/questions/26651/why-is-the-specific-heat-of-water-high Värme [20576] Svar: Energi för att kyla kopparcylindern frĺn 94.0 till 15.4 grader: CCu*m*DT = CCu*0.145*(94.0-15.4) (1) Energi för att värma vattnet frĺn 12.0 till 15.4 grader: Cvatten*m*DT =
4180*0.335*(15.4-12.0) (2) Om vi sätter (1) lika med (2) fĺr vi: CCu = 4180*0.335*(15.4-12.0)/(0.145*(94.0-15.4)) = 418 J/(kg*K) Detta stämmer dĺligt med det korrekta värdet 385 J/(kg*K) frĺn
Heat_capacity#Table_of_specific_heat_capacities Se även Pluggakuten, länk 1. Observera att den första lösningen är fel, men den andra är korrekt. Nyckelord: specifik värmekapacitet [25]; 1 https://gamla.pluggakuten.se/forumserver/viewtopic.php?id=123363&id=123363 Värme [19531] Svar: Vatten har alltsĺ den specifika värmekapaciteten 4181 J/(kg*K) och järn 450 J/(kg*K). Vatten är alltsĺ kilo för kilo 10 gĺnger mer effektivt än järn. Om i stället volymen hade varit avgörande skulle skillnaden vara betydligt mindre pĺ grund av järnets höga densitet. Tar man hänsyn till att järn kan värmas till betydligt högre temperatur blir järn mer effektivt som värmekälla. Vatten har, som synes i tabellen, bland den största specifika värmekapaciteten av alla ämnen. Nyckelord: specifik värmekapacitet [25]; Elektricitet-Magnetism [19430] Ursprunglig frĺga: Svar: Supraledning finns vid tillräckligt lĺga temperaturer hos vissa metaller och även keramiska ämnen. Det finns ämnen som är supraledande vid sĺ hög temperatur att man kan använda billigt och lättillgängligt flytande kväve som kylmedel (kokpunkt 77 K). Supraledning är ganska komplext och det finns olika förklaringar och fenomenet är inte helt förstĺtt, speciellt när det gäller högtemperatursupraledare. Den klassiska förklaringen är BCS-teorin (se BCS_theory I en vanlig ledare (typiskt en metall) sker laddningstransporten med fria elektroner, se frĺga 9549 I vissa ledare vid lĺg temperatur slĺr sig elektronerna ihop tvĺ och tvĺ med motsatt spinn (+1/2.-1/2). Man fĺr dĺ vad man kallar ett Cooper-par med spinnet 0. Dessa Cooper-par leder strömmen i stället för fria elektroner. Pĺ grund av kvantmekaniken är den emellertid tvĺ avgörande skillnader: 1 Eftersom ett Cooper-par har heltaligt spinn (0) är de bosoner och behöver till skillnad frĺn fermioner (halvtaligt spinn) inte lyda pauliprincipen, se frĺga 18298 2 Energin i grundtillstĺndet är för liten för att Cooper-paren skall kunna växelverka med gittret. Detta betyder att kollisioner blir "förbjudna" och Cooper-paren kan röra sig obehindrat, det vill säga att resistansen är noll. I figuren nedan visas resistiviteten (grön kurva) som funktion av temperaturen. Man ser att resistiviteten är exakt noll för temperaturer mindre än Tc. Den blĺ kurvan visar specifik värmekapacitet. Man ser att även denna pĺverkas vid fasövergĺngen T=Tc. Se även Superconductivity Nyckelord: supraledning [7]; pauliprincipen [10]; resistans [15]; specifik värmekapacitet [25]; Bose-Einstein-kondensat [6]; Värme [19315] Ursprunglig frĺga: Svar: En bassäng med vatten har mycket stor värmekapacitet, sĺ det krävs mycket energi för att värma upp den. Lĺt oss anta följande: Bassängens volym: 6x4x1.5 = 36 m3 Energi för att värma vattnet en grad: 4200*36*1000*1 = 151200000 = 1.5*108 J Om vi vill värma vattnet 2 grader per dygn behöver vi effekten: 2*151200000/(24*60*60) = 3500 W = 3.5 kW Nyckelord: specifik värmekapacitet [25]; Värme [19279] Detta är enkelt med formeln E=cmΔT för bägaren med bara vatten. Men hur bestämmer man energin dĺ även en metall absorberar värme? hur nyttjar man formeln dĺ det finns olika ämnen och alltsĺ mer än en värmekapacitet? Svar: E = c*m*ΔT + cm*mm*ΔT cm, metallens specifika värmekapacitet, hittar du i Specific_heat_capacity#Table_of_specific_heat_capacities Nyckelord: specifik värmekapacitet [25]; Värme [19001] Ursprunglig frĺga: Svar: Först nĺgra definitioner: Gaskonstanten (i allmänna gaslagen): R = 8.3145 J/(mol*K) Boltzmanns konstant: k = 1.38065*10-23 J/K Avogadros tal: NA = 6.02214*1023 /mol R = k*NA (k hänför sig alltsĺ till en molekyl och R hänför sig till en mol, dvs NA molekyler) För fasta ämnen och vätskor är det inte helt lätt, men lĺt oss börja med en gas eftersom det är lättare att förstĺ. Figuren nedan (frĺn Heat_capacity Varje frihetsgrad har värmekapaciteten (1/2)R J/mol eller (1/2)k J/partikel. Lĺt oss betrakta en tvĺatomig gas, se figuren nedan. Molekylen kan röra sig i tre riktningar x,y och z. Vi har alltsĺ 3 frihetsgrader och värmekapaciteten vid lĺga temperaturer blir (3/2)R. Vid lite högre temperaturer kommer nya frihetsgrader in för en tvĺatomig gas (för en enatomig gas förblir värmekapaciteten (3/2)R). Först rotation. En tvĺatomig molekyl kan rotera kring tvĺ axlar. Den tredje axeln är linjen mellan de tvĺ atomerna, och den kommer inte i frĺga av kvantmekaniska skäl (symmetri). Vi har alltsĺ ytterligare tvĺ frihetsgrader, och vid normala temperaturer är CV = (5/2)R. (Figuren är lite missvisande här eftersom detta är temperaturomrĺdet en tvĺatomig gas normalt befinner sig i.) Vid ytterligare högre temperatur kommer även vibrationer in. Molekylen kan vibrera längs axeln som definieras av linjen mellan atomerna. Denna vibration har tvĺ frihetsgrader (potentiell energi och kinetisk energi), sĺ CV = (7/2)R. Vad händer dĺ med fasta ämnen/vätskor? Alla atomer binds till sina närmaste grannar. Vi bör alltsĺ ha tre vibrationstillstĺnd (x, y och z) med tvĺ frihetsgrader var (potentiell energi och kinetisk energi). CV bör alltsĺ vara 3*2* (1/2)R = 3R Detta kallas Dulong-Petits lag. Denna stämmer ganska väl för de flesta ämnen. Det tillkommer emellertid ett par komplikationer. För vissa ämnen, speciellt lätta ämnen med starka bindningar som C och Be, är vissa av vibrationstillstĺnden blockerade vid rumstemperatur eftersom excitationsenergin är för hög. Värmekapaciteten blir dĺ lägre än 3R. Dessutom är det antalet atomer som bestämmer CV. I tabellen Heat_capacity#Table_of_specific_heat_capacities Eftersom vibrationstillstĺnden inte kan exciteras vid lĺg energi brukar CV för fasta ämnen gĺ mot noll när temperaturen gĺr mot noll. Se även frĺga 17968 Nyckelord: specifik värmekapacitet [25]; gaslagen, allmänna [24]; Värme [18803] Svar: (10 m2)*(5*3600 s)*(0.600 kJ/(s*m2)) = 108000 kJ. Vattnet i bassängen värms upp x grader. Specifika värmekapaciteten för vatten är 4.18 kJ/(kg*K). Energin som gĺr ĺt är dĺ (x K)*(10*4*1.4 m3)*(1000 kg/m3)*4.18 kJ/(kg*K)) = x* kJ = 234000 kJ. Om vi sätter detta lika med energin frĺn solfĺngaren fĺr vi x = 108000/234000 K = 0.46 K. Detta lĺter lite, men observera att bassängen innehĺller mycket vatten och vattnets värmekapacitet är mycket stor. Om vi kan köra systemet fullt ut under tre mĺnader pĺ sommaren blir energiinnehĺllet 108000*90 = 9700000 kWs = (9700000 kWs)/(3600 s/h) = 2700 kWh. En välisolerad villa kräver c:a 15000 kWh för uppvärmning. Man behöver alltsĺ ĺtminstone 40 m2 solfĺngare snarare än 10 m2. Nyckelord: specifik värmekapacitet [25]; solenergi [14]; Värme [18740] Jag vill räkna ut hur mycket Q (VÄRMEMÄNGD) vattnet upptagit, och vikten angivit?
Med hjälp av de har jag fĺtt ihop olika värdena. Vattens massa: 0,3 liter Stĺlens massa: 0,1kg Tack sĺ hemskt mycket! Svar: Din beskrivning av försöket lämnar lite övrigt att önska! Jag antar du stoppar en uppvärmd stĺlbit i en bägare med vatten. Vattnets temperatur mäts före och efter. Du skall räkna ut hur mycket värme som upptas av vattnet (lika mycket som avges av stĺlbiten). Beräkna även stĺlbitens temperatur innan den las ner i vattenbägaren. Med de värden du ger blir av vattnet upptagen värme 0.3*4.16*(25-23) = 2.5 J Om stĺlets begynnelsetemperatur är T fĺr vi 2.5 = 0.1*0.46*(T-25) vilket ger T = 25 + 2.5/(0.1*0.46) = 25 + 54 = 79oC Det är fel i dina uppgifter: specifika värmekapaciteten är given i kJ/(kg*K) men eftersom detta gäller bĺde stĺl och vatten har det ingen betydelse för sluttemperaturen T. Av vattnet upptagen och av stĺlet avgiven värme skall emellertid vara 2.5 kJ eller 2500 J! Sluttemperaturen är samma i vattnet som i stĺlet, 25 grader. Nyckelord: specifik värmekapacitet [25]; Värme [18574] Är otroligt tacksam för ett sĺ snabbt svar som möjligt :)) Svar: Ditt värde 5000/0.986 = 5070 J är inte särskilt nära det korrekta värdet pĺ vattnets specisfika värmekapacitet, 4200 J/(kg*K). Anledningen är att du inte har räknat med värmekapaciteten för termosen. Du behöver alltsĺ mer information för att lösa problemet. För att bestämma ĺngbildningsvärmet mĺste du även väga mängden vatten som kokar bort. Temperaturen under förĺngningsfasen bör vara konstant. Nyckelord: specifik värmekapacitet [25]; Värme [17968] jag undrar om det finns nĺgot direkt samband mellan värmekapacitet och värmekonduktivitet för olika ämnen. T.ex. vatten som har hög värmekapacitet men lĺg värmekonduktivitet. Vad avgör hur hög värmekonduktivitet ett ämne har? Tack pĺ förhand Svar: Vad gäller värmekonduktivitet sĺ är den i stort sett proportionell mot den elektriska konduktiviteten. Detta eftersom bĺde ström och värme transporteras av elektroner, sĺ det är dessas antal och rörlighet som är viktigt. Se Heat_conductivity#Electrical_conductivity Nyckelord: specifik värmekapacitet [25]; värmeöverföring/transport [46]; Värme [17805] Svar: Nyckelord: *vardagsfysik [64]; specifik värmekapacitet [25]; Energi [17697] Ursprunglig frĺga: Svar: Specifika värmekapaciteten C för vatten är 4180 J/kg.K, se frĺga 14203 mgh = mCDT dvs DT = gh/C = 10*100/4180 = 0.24 K. Dimensionskontroll: [(m/s2)*m/(N*m)/(kg*K)] =
[(m2/s2)/(kg*m/s2*m)/(kg*K)] = [1/1/(K)] = [K] Detta torde vara knappt mätbart! Nyckelord: vattenkraft [7]; specifik värmekapacitet [25]; potential/potentiell energi [30]; dimensionsanalys [7]; Värme [17491] Svar: Lĺt oss räkna pĺ en kulstötningskula. Den väger 7.26 kg (Kulstötning För att värma upp kulan frĺn 20 grader till 100 grader krävs energin DQ = 7.26*449*80 = 2.6 105 J Frĺn E = mc2 fĺr vi massdifferensen Dm = 2.6 105/(3 108)2 = 2.9 10-12 kg vilket torde vara omätbart! Se vidare Special_relativity#Equivalence_of_mass_and_energy Nyckelord: relativitetsteorin, speciella [45]; specifik värmekapacitet [25]; Ljud-Ljus-Vĺgor [16880] Ursprunglig frĺga: Svar: Mikovĺgorna hĺlls innne i ugnen genom att den är konstruerad som en faradaybur (se frĺga 8879 Se frĺga 16041 Se frĺga 3969 Hur man kontrollerar effekten hos en mikrovĺgsugn När mikrovĺgsugnen blir gammal blir magnetronen som genererar mikrovĺgorna mindre effektiv, och det tar längre tid att värma maten. Sĺ här kan du kontrollera hur effektiv din mikrovĺgsugn är. Du behöver bara en skĺl (glas eller keramik) med 1 liter kallt vatten och en hyggligt exakt termometer. Mät temperaturen pĺ vattnet. Säg att vattnet är 20oC. Kör ugnen 1 minut. Mät vattentemperaturen igen. Säg att vattnet nu är 30oC. Sedan fĺr vi räkna lite för att fĺ fram effekten. Energin som krävs för att värma vattnet DT K är: W = m*c*DT där m är massan och c är vattnets specifika värmekapacitet 4180 J/(kg K). Om vi kör mikron under tiden t fĺr vi effekten P = W/t = m*c*DT/t 1 liter vatten väger 1 kg, sĺ effekten blir P = 4180*DT/t Om vi körde mikron 1 minut och temperaturskillnaden var 10 K (eftersom vi har att göra med temperaturskillnader kan vi använda Celsius eller Kelvin) blir effekten P = 4180*10/60 = 697 W Om temperaturdifferensen blir liten bör man öka tiden t för att fĺ bättre noggrannhet. Den uppmätta effekten jämförs sedan med den nominella effekten enligt bruksanvisningen. Man kan även mäta in-effekten direkt med en wattmeter (se Watt_meter Om ovanstĺende är för krĺngligt kan man om man har en "standardportion", t.ex. ett fruset halvt franskbröd, helt enkelt se om upptiningen tar längre tid än vanligt.
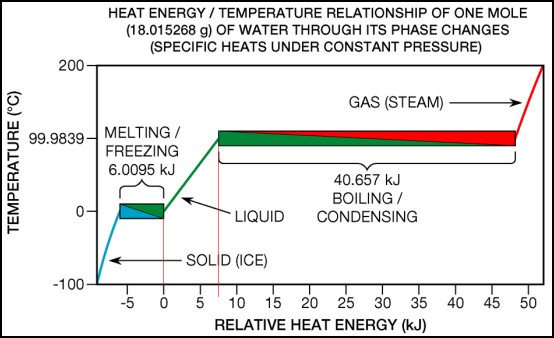
Nyckelord: mikrovĺgsugn [25]; specifik värmekapacitet [25]; *vardagsfysik [64]; Värme [16374] Ursprunglig frĺga: Svar: För att höja gommens temperatur krävs dels att pizzan har tillräcklig specifik värmekapacitivitet och dels att värmeledningsförmĺgan är tillräcklig (och naturligtvis att den är tillräckligt varm). Sĺ svaret är alltsĺ: bĺde och! Om värmeledningsförmĺgan är dĺlig, är det bara ett tunnt skikt som bidrar: liten temperaturhöjning eftersom temperatursänkningen hos pizzan är stor. Om specifika värmekapacitiviteten är liten, fĺr man igen en stor sänkning av pizzans temperatur. Metaller har mycket hög värmeledningsförmĺga (eftersom det finns fria elektroner) och rimligt hög specifik värmekapacitivitet (värmemängd per kg och K). Man bränner sig alltsĺ mycket pĺ metaller. Du bränner dig pĺ spiken i bastun men inte pĺ trätrallorna. Du bränner dig inte heller pĺ en het aluminiumfolie, eftersom massan är sĺ liten och därmed värmekapaciteten. Vatten har mycket hög specifik värmekapacitivitet och hygglig värmeledningsförmĺga. Torra bitar som brödet har emellertid lĺg värmekapacitivitet och dĺlig värmeledningsförmĺga eftersom brödet innehĺller en massa luftbubblor som leder värme dĺligt. Det är alltsĺ pĺ fyllningen (som innehĺller mycket vatten) och inte pĺ brödet du bränner dig. /*fa* Nyckelord: värmemängd [3]; värmeöverföring/transport [46]; specifik värmekapacitet [25]; *vardagsfysik [64]; Värme [16294] Svar: Om man vill lagra värme är det naturligtvis bra om om den specifika värmekapaciteten är hög, dvs mĺnga joule per kg och grad temeraturändring. Vatten har dessa egenskaper (se frĺga 14203 nedan) och används därför ofta som lagringsmedium. Jag tror inte man i större omfattning använder fasomvandling för energilagring, det används däremot i kylskĺp och värmepumpar. Eftersom temperaturerna i lagringsmediet normalt är ganska lĺga och det krävs en temperatur pĺ minst 40-50 grader för att ĺstadkomma uppvärmning av t.ex. ett hus, sĺ använder man vanligtvis en värmepump, se frĺga 14245 nedan. Atomers och molekylers förmĺga att lagra energi är, som ni säger, beroende av egenskaper hos de kemiska bindningarna. Se vidare Thermal_energy_storage Se även frĺga 14203 Nyckelord: specifik värmekapacitet [25]; energilagringssystem [7]; Värme [15734] Ursprunglig frĺga: Svar: Se pĺ figuren för vatten nedan (frĺn Wikipedia-artikeln Thermodynamic_temperature 40.7 kJ/mol = 1000*40.7/18 = 2260 kJ/kg. Pĺ samma sätt blir smältvärmet för is 6.01 kJ/mol = 1000*6.01/18 = 334 kJ/kg. Frĺn lutningen (egentligen 1/lutningen) hos den räta linjen mellan is och ĺnga kan man räkna ut den specifika värmekapaciteten för vatten: 7.5 kJ/(mol*K) = 1000*7.5/(18*100) = 4.2 kJ/(kg*K) Det faktum att kurvan i detta omrĺde är en rät linje reflekterar det faktum att specifika värmekapaciteten för vatten är oberoende av temperaturen. Detta gäller approximativt för de flesta ämnen. Sedan är jag inte helt klar över vad du menar att kurvan inte är konstant. I de horisontella omrĺdena (vid smältpunkten 0oC och vid kokpunkten 100oC) ändras inte temperaturen om bara tillförseln av värmet sker pĺ ett effektivt sätt. Dĺ har hela provet en konstant temperatur och all tillförd värme gĺr till att ändra aggregationstillstĺnd. Den gröna kurvan mellan is och ĺnga representerar alltsĺ den specifika värmekapaciteten för vatten. Det faktum att kurvan är mycket nära en rät linje betyder helt enkelt att vattens specifika värmekapacitet är konstant mellan 0oC och 100oC. Detta gäller inte allmänt - andra ämnen kan ha olika olinjära kurvor. Man ser även pĺ den blĺ kurvan till vänster (för is) att den avviker frĺn en rät linje. Lägg ocksĺ märke till att den blĺ kurvan har ungefär dubbelt sĺ stor lutning som den gröna (för vatten). Detta betyder att specifika värmekapaciteten för is är ungefär hälften av den för vatten. Nyckelord: specifik värmekapacitet [25]; Värme [15290] Svara gärna hur ni har gjort hela vägen sĺ jag förstĺr! Tack sĺ jättemycket! Svar: Energin som gĺr ĺt för att höja temperaturen till 37 grader hos det kalla vattnet är x*(37-8)*k där k är specifik värmekapacitet (200-x)*(65-37)*k när det vama vattnet kyls till 37 grader. Värmen som gĺr ĺt att värma det kalla vattnet tas frĺn det varma. Om vi antar att inget energiutbyte sker med omgivningen är de tvĺ uttrycken ovan lika och vi fĺr en enkel ekvation med en obekant: x*(37-8)*k = (200-x)*(65-37)*k x*29 = (200-x)*28 29x = 28*200 - 28x 57x = 28*200 x = 28*200/57 = 98.2 Vi skall alltsĺ ta 98.2 liter kallvatten och (200-98.2)=101.8 liter vamvatten. Nyckelord: specifik värmekapacitet [25]; Värme [14203] Svar:
Uppvärmning -15->0
Ĺterstĺr alltsĺ 16.488 - 1.575 kJ = 14.913 kJ för att smälta x kg is: x*333 = 14.913 kJ, vilket ger x = 14.913/333 = 0.04478 kg = 45 g. Du har nog glömt att ta hänsyn till värmekapaciteten hos termosen, det är ungefär 10% av vattnets. Här är data för nĺgra vanliga ämnen: Jämfört med andra ämnen har vatten högt smältvärme, hög specifik värmekapacitet och mycket hög ĺngbildningsvärme. Detta beror dels pĺ vattnets lĺga molekylvikt (innehĺller mĺnga molekyler per kg) och pĺ de vätebindningar som finns mellan närliggande molekyler pga att vattenmolekylen är en dipol. En del av energin gĺr alltsĺ ĺt för att bryta upp vätebindningar snarare än att "sätta fart" pĺ molekylerna. Water Structure and Science Nyckelord: vatten/is [49]; specifik värmekapacitet [25]; Värme [8869] Svar: Se även frĺga 5233 Nyckelord: specifik värmekapacitet [25]; Värme [4888] Svar: Vatten är mycket effektivare för värmeöverföring än luft. Det beror pĺ vattnets högre värmekapacitet, högre värmeledning och att strömningen blir intensiv vid kokning. Luft har mycket lägre värmekapacitet och värmeöverföringen luft-potatis är ineffektiv. Se även frĺga 16152 Tänk pĺ: Man kan sitta en god stund i en torrbastu vid 100 grader, men man tĺl absolut inte kokande vatten. Nyckelord: specifik värmekapacitet [25]; värmeöverföring/transport [46]; Frĺgelĺdan innehĺller 7624 frĺgor med svar. ** Frĺgelĺdan är stängd för nya frĺgor tills vidare **
|




 Sök i svenska Wikipedia:
Sök i svenska Wikipedia:
