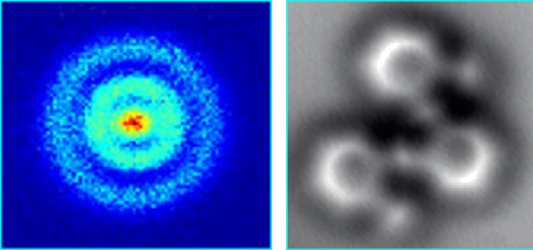
Vill du ha ett snabbt svar - sök i databasen: Anpassad Google-sökning 9 frĺgor/svar hittade Materiens innersta-Atomer-Kärnor [20583] Svar: Till skillnad frĺn excitation med fotoner är kravet för oelastisk spridning av elektroner inte att energin skall vara lika med energidifferensen mellan grundtillstĺndet och ett exciterat tillstĺnd. För att fĺ en mätbar sannolikhet mĺste den inkommande elektronen ha en energi som är större än energiskillnaden mellan grundtillstĺndet och det exciterade tillstĺndet. Energin som "blir över" tas om hand av den utgĺende elektronen och det exciterade tillstĺndet sönderfaller genom att sända ut en foton, se nedanstĺende bild. Oelastisk spridning av elektroner pĺ fria atomer var ett mycket direkt stöd för Bohrs atommodell: Franck-Hertz försök var ett fysikexperiment som stöder Bohrs atommodell, en föregĺngare till kvantmekanik. De tyska fysikerna James Franck och Gustav Hertz försökte 1914 undersöka energinivĺerna i en atom. Deras numera berömda experiment stödde pĺ ett elegant sätt Niels Bohrs atommodell där elektroner rör sig runt atomkärnan i banor med specifika diskreta energier. Franck och Hertz fick 1925 Nobelpriset i fysik för detta arbete. Franck-Hertz försök bekräftade Bohrs kvantiserade atommodell genom att visa att atomer bara kan absorbera vissa specifika energimängder (kvanta). (Franck-Hertz_försök Se vidare frĺga 1591 Nyckelord: Bohrs atommodell [9]; Materiens innersta-Atomer-Kärnor [19392] Ursprunglig frĺga: Svar: Bilden nedan till vänster visar en bild pĺ en väteatom framställd med en teknik som kallas kvantmikroskopi (eller fotojonisationsmikroskopi), se länk 1. Man kan se hur elektronen rör sig i ett antal moln pĺ olika avstĺnd frĺn protonen och inte i en planetbana som i Bohrs enkla atommodell. I bilden nedan till höger (länk 2) har man använt atomkraftsmikroskopi (se Atomkraftsmikroskopi En atom har en radie pĺ ungefär 1/10 nanometer, sĺ upplösningen är alltsĺ betydligt bättre än detta. Nobelpriset i kemi för 2014 var för högupplöst avbildning med fotoner: Super-resolution_microscopy Nyckelord: atomradie [8]; elektronskal [12]; Bohrs atommodell [9]; 1 http://io9.com/the-first-image-ever-of-a-hydrogen-atoms-orbital-struc-509684901 Materiens innersta-Atomer-Kärnor [18154] Min frĺga är följande: Har elektronerna alltid bestämda platser runt atomkärnan? När elektronen exiteras är det dĺ samma elektron som hoppar tillbaka och sänder ut ljus eller kan det vara sĺ att en annan elektron frĺn de yttre skalen fyller ut platsen? Svar: Elektronerna har en viss sannoliksfördelning sĺ man kan föreställa sig elektronerna som moln som överlappar med varandra. Alla elektroner är ekvivalenta (identiska) sĺ övergĺngar kan ske med vilken elektron som helst om bara energin kan bevaras och lite andra mer avancerade villkor är uppfyllda. Sĺ vilken elektron som bara befinner sig i ett högre tillstĺnd kan fylla en lägre liggande vakans. Nyckelord: Bohrs atommodell [9]; Materiens innersta-Atomer-Kärnor [16629] Ursprunglig frĺga: Svar: Atomkärnor har 1 till c:a 100 positivt laddade protoner (och ett antal neutroner som vi inte behöver bekymra oss för). För att atomen skall vara oladdad mĺste den ha samma antal negativa elektroner som den har protoner. Detta antal kallas för atomnummer, och bestämmer vilket grundämne vi har att göra med. Enligt kvantmekanik Sammanfattning: Elektronskal är frĺn varandra avgränsade energiintervall inom vilka elektronerna i en atom kan befinna sig. En valenselektron är en elektron i atomens yttersta skal (valensskalet). Antalet valenselektroner har stor betydelse för vilka kemiska föreningar atomen kan ingĺ i, det vill säga antalet bestämmer atomslagets kemiska egenskaper. Alla ädelgaser har strukturen ns2np6 i sitt yttre skal. Undantaget He som ju bara ha tvĺ elektroner 1s2. Gemensamt för alla ädelgaserna är alltsĺ att det yttersta skalet är fullt (2 elektroner i s-tillstĺnd och 6 elektroner i p-tillstĺnd). Nyckelord: elektronskal [12]; Bohrs atommodell [9]; Materiens innersta-Atomer-Kärnor [15971] Svar: Nyckelord: Bohrs atommodell [9]; Materiens innersta-Atomer-Kärnor [14699] Svar: Se även Atomic_theory Nyckelord: vetenskaplig metod [18]; Bohrs atommodell [9]; Materiens innersta-Atomer-Kärnor [13733] Svar: Bohrs atommodell är historiskt mycket viktig, men den ger en alldeles för enkel och felaktig bild av atomen. För att fĺ en bättre bild behöver man använda kvantmekanik. En del av denna är Heisenbergs obestämdhetsrelation som säger att läget av smĺ partiklar som elektroner inte kan bestämmas exakt. Vi bör hellre föreställa oss elektronerna som ett negativt laddat "moln" som omger atomkärnan. Man kan alltsĺ inte säga att elektronbanan har en viss radie, men det är fortfarande sĺ att för högre energitillstĺnd är medelavststĺndet frĺn kärnan i allmänhet större. Jag tycker detta är en bättre bild än "planetmodellen" där elektronerna hoppar frĺn en bana till en annan: Föreställ dig en elektron i ett visst tillstĺnd som ett negativt laddat moln runt atomkärnan. Hur laddningsfördelningen ser ut beror pĺ tillstĺndet. Ett annat tillstĺnd har alltsĺ en annan fördelning av den negativa laddningen. Om atomen gĺr frĺn det ena tillstĺndet till det andra, sĺ ändras laddningsfördelningen. Denna ändring ger upphov till eller absorberar elektromagnetisk strĺlning (ljus). Vilka nivĺer man fĺr i en atom kan man räkna ut genom att lösa den s.k. Schrödingerekvationen (Schrödinger_equation För mer om Bohrs atommodell, se Bohr_model Nyckelord: Bohrs atommodell [9]; Heisenbergs obestämdhetsrelation [12]; kvantmekanik [30]; 1 http://kurslab.fysik.lth.se/Pi/2005/Sammanfattning/Bohr-amodell.pdf Materiens innersta-Atomer-Kärnor [1332] Svar:
Fundera: Antag att du är en skurk i vilda västern. Det kommer
en prärievagn som du tror är lastad med bomull. För att testa detta skjuter
du
hundra skott mot vagnen. 99 skott gĺr rakt igenom vagnen medan ett studsar
tillbaks mot dig. Var vagnen lastad med bomull? Vad tror du vagnen var
lastad med?
Rutherfors experiment liknar mycket exemplet ovan. Han blev väldigt
förvĺnad
när nästan, men inte riktigt, alla alfapartiklarna gick rakt igenom foliet. Han tolkade detta
som att
nästan allt är tomrum men att det finns smĺ, men mycket tunga atomkärnor
mitt inne i atomen.
Det var han som formulerade atommodellen som säger att det finns en liten
men tung kärna i mitten. Han fick Nobelpriset i kemi 1908 för tidigare arbeten om sönderfall av atomkärnor, se The Nobel Prize in Chemistry - Laureates Nyckelord: Bohrs atommodell [9]; Materiens innersta-Atomer-Kärnor [1315] Svar:
Analogi Man placerar elektronerna i atomens elektronskal ungefär
som böcker i en bokhylla. Pĺ varje plats fĺr det bara rum en bok.
Varje elektron har fyra olika kvanttal: n, l, m, ms.
Det är svĺrt att ge en exakt definition av dem pĺ "gymnasiefysiknivĺ". Istället
fĺr vi ge en enkel bild enligt Bohrs atommodell.
n betecknar antalet nollställen i den radiella vĺgfunktionen + 1.
l anger hur utdragen banan är.
m anger hur banans plan lutar.
ms anger om spinnet är upp eller ner.
Ett röntgenspektrum uppkommer om man lyckas ta bort en elektron frĺn ett inre skal
i atomen. När nĺgon av de yttre elektronerna "hoppar in" till den tomma platsen
sĺ sänds en röntgenfoton ut. Nyckelord: Bohrs atommodell [9]; pauliprincipen [10]; elektronskal [12]; Frĺgelĺdan innehĺller 7624 frĺgor med svar. ** Frĺgelĺdan är stängd för nya frĺgor tills vidare **
|



 Sök i svenska Wikipedia:
Sök i svenska Wikipedia:
