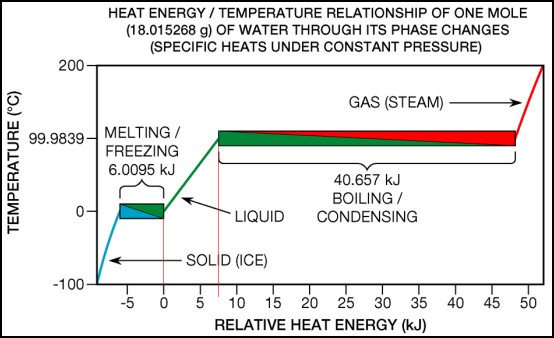
Värme [15734] Ursprunglig frĺga: Svar: Se pĺ figuren för vatten nedan (frĺn Wikipedia-artikeln Thermodynamic_temperature 40.7 kJ/mol = 1000*40.7/18 = 2260 kJ/kg. Pĺ samma sätt blir smältvärmet för is 6.01 kJ/mol = 1000*6.01/18 = 334 kJ/kg. Frĺn lutningen (egentligen 1/lutningen) hos den räta linjen mellan is och ĺnga kan man räkna ut den specifika värmekapaciteten för vatten: 7.5 kJ/(mol*K) = 1000*7.5/(18*100) = 4.2 kJ/(kg*K) Det faktum att kurvan i detta omrĺde är en rät linje reflekterar det faktum att specifika värmekapaciteten för vatten är oberoende av temperaturen. Detta gäller approximativt för de flesta ämnen. Sedan är jag inte helt klar över vad du menar att kurvan inte är konstant. I de horisontella omrĺdena (vid smältpunkten 0oC och vid kokpunkten 100oC) ändras inte temperaturen om bara tillförseln av värmet sker pĺ ett effektivt sätt. Dĺ har hela provet en konstant temperatur och all tillförd värme gĺr till att ändra aggregationstillstĺnd. Den gröna kurvan mellan is och ĺnga representerar alltsĺ den specifika värmekapaciteten för vatten. Det faktum att kurvan är mycket nära en rät linje betyder helt enkelt att vattens specifika värmekapacitet är konstant mellan 0oC och 100oC. Detta gäller inte allmänt - andra ämnen kan ha olika olinjära kurvor. Man ser även pĺ den blĺ kurvan till vänster (för is) att den avviker frĺn en rät linje. Lägg ocksĺ märke till att den blĺ kurvan har ungefär dubbelt sĺ stor lutning som den gröna (för vatten). Detta betyder att specifika värmekapaciteten för is är ungefär hälften av den för vatten. Nyckelord: specifik värmekapacitet [25]; Frĺgelĺdan innehĺller 7624 frĺgor med svar. ** Frĺgelĺdan är stängd för nya frĺgor tills vidare **
|